Akademia Wychowania Fizycznego im. Eugeniusza Piaseckiego w Poznaniu, Poznań 2003.
Spis treści
- PRZEDMOWA
- I. WALORY KLIMATYCZNE TERENÓW LUDWIKOWA I KRÓTKA HISTORIA SZPITALA
- II. CHOROBY UKŁADU ODDECHOWEGO I ICH ZNACZENIE W XXI WIEKU
- III. USPRAWNIANIE RUCHOWE JAKO ELEMENT LECZENIA W PNEUMOLOGII
- IV. REHABILITACJA PSYCHOLOGICZNA – NIEZBĘDNE OGNIWO W KOMPLEKSOWYM LECZENIU W LUDWIKOWIE
- V. DOBÓR CHORYCH DO PROWADZENIA REHABILITACJI ODDECHOWEJ I OCENA ICH WYDOLNOŚCI FIZYCZNEJ
- VI. TRENING FIZYCZNY JAKO PODSTAWA W SYSTEMIE REHABILITACJI PNEUMOLOGICZNEJ
- VII. USPRAWNIANIE RUCHOWE W WYBRANYCH SCHORZENIACH PŁUC
- VIII. STRUKTURA ORGANIZACYJNA SZPITALA W LUDWIKOWIE
- LITERATURA
Spis rysunków
- Dyrektor Szpitala – dr n. med. Aleksander Barinow-Wojewódzki
- Archiwalne zdjęcie z 1900 r. – Pawilon I
- Pawilon leczniczy nr II przy ul. Parkowej
- Ludwikowo z lotu ptaka
- Mapa usytuowania Szpitala
- Pawilon leczniczy nr I od strony ul. Leśnej
- Pawilon leczniczy nr I od strony leżakowni
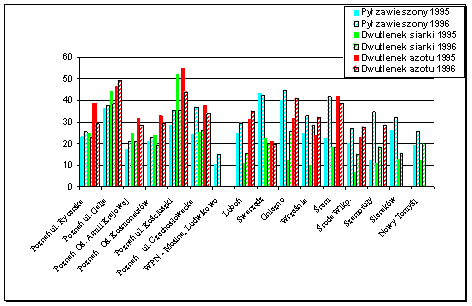
- Stężenia zanieczyszczeń powietrza w różnych regionach województwa wielkopolskiego
- Centralna tlenownia (wybudowana w 2000 r.)
- Pracownia RTG
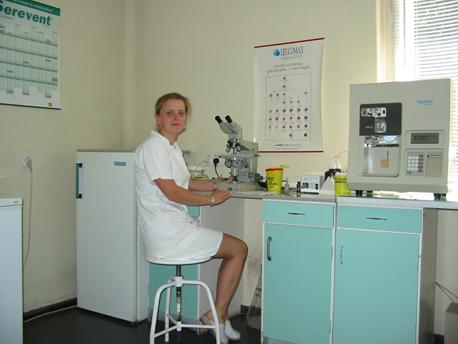
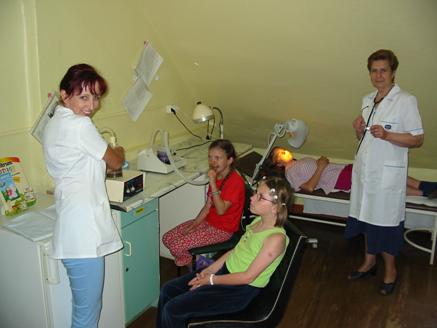
- Pracownia spirometryczna
- Inhalatornia w Pawilonie leczniczym nr II
- Laboratorium analityczne – część gazometryczna
- Trening wytrzymałościowy na ergometrze
- Laboratorium analityczne – część hematologiczna
- Transport sanitarny przewożący pacjentów do naświetlań w Wielkopolskim Centrum Onkologii w Poznaniu
- Laboratorium bakteriologiczne – pracownia prątka gruźlicy
- Apteka szpitalna
- Trening wytrzymałościowy na bieżni
- Gabinet stołów do masażu z napędem elektrycznym – część A
- Sala gimnastyczna nr 2 – ćwiczenia rozciągające
- Gabinet stołów do masażu z napędem elektrycznym – część B
- Sala konferencyjna w Pawilonie leczniczym nr I
- Sala posiedzeń w Pawilonie leczniczym nr I
- Kaplica szpitalna
- Figura Matki Boskiej Niepokalanej
- Sala gimnastyczna nr 2 – ćwiczenia grupowe kończyn górnych
- Gimnastyka oddechowa na świeżym powietrzu
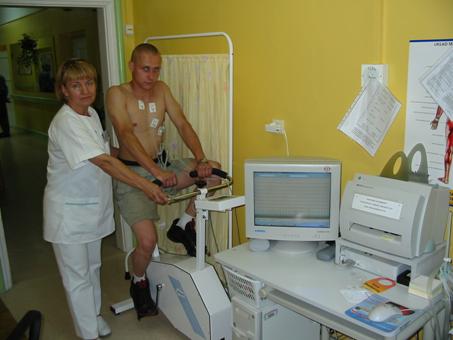
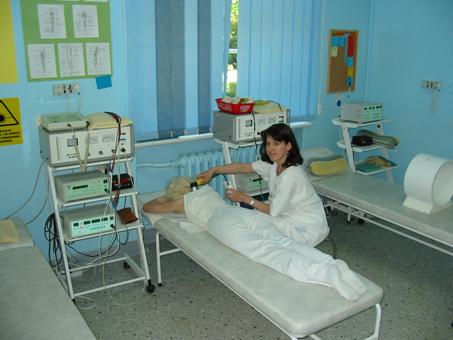
- Pracownia testów wysiłkowych
- Sala gimnastyczna nr 2 – ćwiczenia korekcyjne
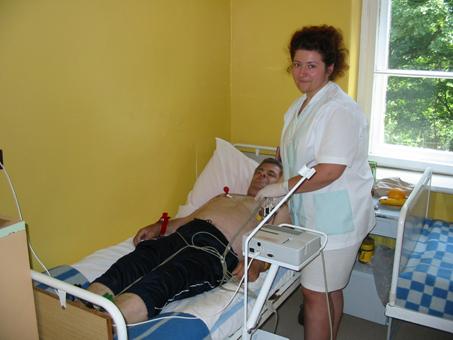
- Pracownia EKG
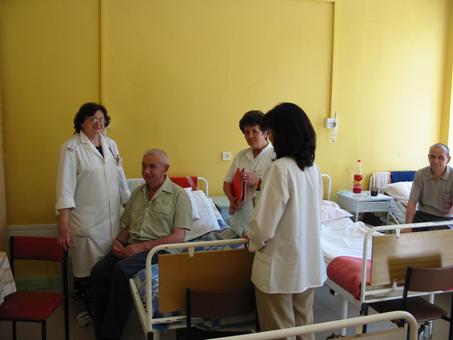
- Wizyta lekarska na oddziale
- Gabinet fizjoterapii – ultradźwięki
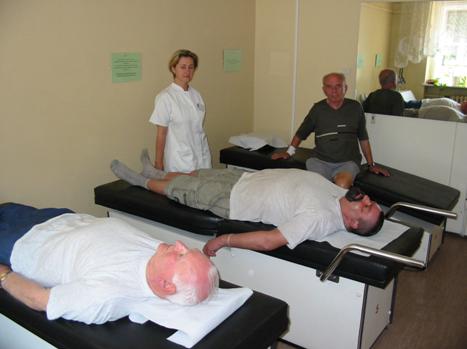
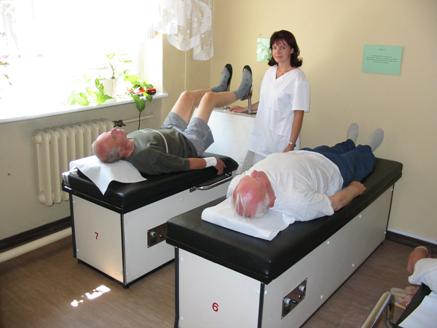
- Drenaż ułożeniowy na stole drenażowym
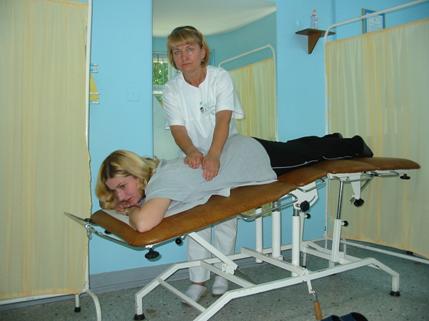
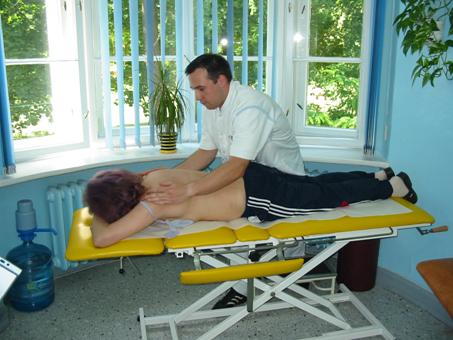
- Masaż leczniczy
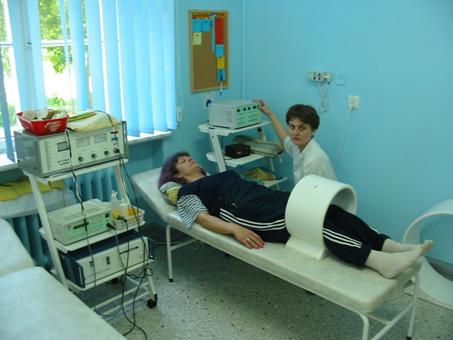
- Gabinet fizjoterapii – magnetoterapia
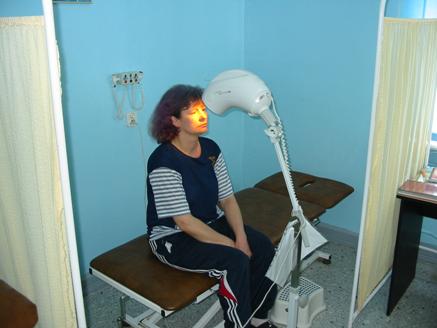
- Gabinet fizjoterapii – lampa biotron
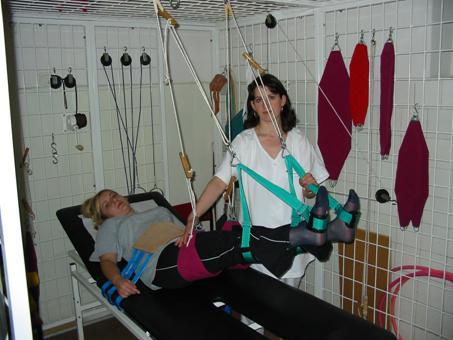
- Sala rehabilitacyjna nr 1 – ćwiczenia w UGUL-u w odciążeniu
- Plan sytuacyjny Ludwikowa przy wjeździe na teren Szpitala
- Budynek Administracji – Dyrekcja Szpitala
- Tablica pamiątkowa
- Pracownia fizjoterapii przy oddziale dziecięcym
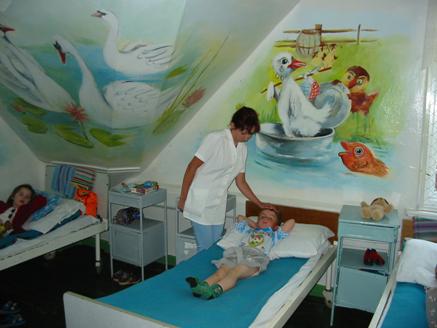
- Sala chorych dla młodszych dzieci
- Kiosk spożywczy
- Figura Serca Jezusowego
- Pijalnia wody źródlanej „Ludwiczanka”
- Brama wjazdowa do Szpitala i budynek portierni
- Punkt konsultacyjny z pracownią USG
Chorobyukładu oddechowego stanowią istotny, często niedoceniany problem medycyny. W minionym dziesięcioleciu pojawiły się nowe metody diagnostyki, leczenia, zapobiegania i rehabilitacji w pneumologii.
Zanieczyszczenie gleby, wód, powietrza, pojawienie się nowych zmutowanych, opornych na tradycyjne leczenie drobnoustrojów, wirusów wymagają poświęcenia większej uwagi chorobom układu oddechowego. Wystarczy spojrzeć na wzrost zachorowań na gruźlicę wielolekooporną albo na zanotowaną w tym roku epidemię ostrej niewydolności oddechowej (SARS) na Wschodzie.
W tym kontekście nabiera znaczenia nie tylko diagnostyka i leczenie, ale i aktualne kreowanie procesu rekonwalescencji w chorobach układu oddechowego. Zwłaszcza w chorobach tradycyjnie nie zaliczanych do jednostek nozologicznych, w których usprawnianie ruchowe było zalecane, a do takich należą: choroba nowotworowa, mukowiscydoza, choroby śródmiąższowe płuc.
Rehabilitacja pneumologiczna z wąskiej specjalizacji stosowanej w obturacyjnej chorobie płuc rozwinęła się w wieloaspektowy kierunek obejmujący farmakoterapię, usprawnienia ruchowe, edukację chorego i rehabilitację psychospołeczną. Celem takiego postępowania jest ciągła poprawa jakości życia pacjentów dotkniętych chorobami układu oddechowego i w miarę możliwości przywrócenie ich zdrowemu społeczeństwu.
Mam nadzieję, że niniejsze opracowanie przybliży Czytelnikom te interesujące i trudne problemy. Jednocześnie pogłębi wiedzę o specjalistycznym ośrodku, gdzie systematycznie wdrażany jest opisany program wieloaspektowego usprawniania w chorobach układu oddechowego.
Od ponad 100 lat Ludwikowo służy Wielkopolanom jako miejscowość uzdrowiskowa, charakteryzująca się szczególnymi cechami klimatycznymi, w stopniu znacznym przyczyniającymi się do leczenia chorób układu oddechowego.
Historia Ludwikowa jest fascynująca. „Ludwikowa Góra” (Ludwigshohe), obecnie Góra Staszica, wyniesiona znacznie w stosunku do otoczenia (113 m n.p.m.), o wyjątkowych walorach klimatycznych, stała się w marcu 1899 r. własnością spółki „Die Gesellschaft Luftkurort und Willenanlage Ludwigshohe”. Z tą datą i z tą spółką należy wiązać początki uzdrowiska w Ludwikowie. Zapewne do połowy 1902 r. wzniesiony został główny budynek i sąsiadujące z nim drewniane werandy, tworzące prostokątny dziedziniec-ogród.
Obiekty powstałe w latach 1898-1902 stanowiły zasadniczą część ówczesnego zespołu. Był to wtedy kurort borykający się zapewne z kłopotami. W 1906 r. nabył go Albert Hoene, kupiec i właściciel hoteli z Poznania.
W czerwcu 1908 r. spółka: „Sanatoriums und Siedlung Genossenschaft Ludwigshohe” zwróciła się z apelem do „wszystkich myślących ludzi Wschodu” o poparcie inwestycji mającej na celu rozwój tego miejsca zdrowia i wypoczynku. Zarząd spółki wyrażał zamiar urządzenia na swoim terenie kolonii drzew owocowych na wzór Edenu koło Oranienburga.
Dzieje obiektu w czasie I wojny światowej nie są znane. W 1919 r. zespół nabyło towarzystwo – firma z Wiesbaden. W lipcu 1920 r. przeszedł w ręce polskie – jako właściciel wymieniona jest „Staszycówka”, zapisana jako spółka z ograniczoną odpowiedzialnością w Poznaniu. Od 25 kwietnia 1923 r. właścicielem był Polski Bank Handlowy, Towarzystwo Akcyjne. W 1924 r. obiekty uzdrowiska dzierżawiły Zofia Chrzanowska i jej siostra. W lipcu 1925 r. jako właściciel wpisany został Okręgowy Związek Kas Chorych na Województwa Poznańskie i Pomorskie. W 1926 r. przeprowadzone były w głównym gmachu prace remontowe – założono centralne ogrzewanie; przebudowano też północną część – zlikwidowano drewniane balkony i przedłużono budynek na długość dwóch sal jadalnych w przyziemiu, z wielką werandą na piętrze.
W 1933 r. na podstawie Rozporządzenia Prezydenta RP z 27 października 1932 r. (Dz.U. poz. 814) właścicielem sanatorium został Związek Kas Chorych z siedzibą w Warszawie.
W połowie września 1939 r. hitlerowcy wykwaterowali chorych, po czym zorganizowali zakład wychowawczo-wynaradawiający dla dziewczynek w wieku 3-12 lat, który działał do 1942 r. Następnie założono w Ludwikowie sanatorium chorób płuc dla dorosłych „Heilstatte Ludwigshohe”. Od stycznia do połowy maja 1945 r. znajdował się tu szpital wojskowy armii radzieckiej. Na początku października 1945 r. zaczęto organizować sanatorium dla dzieci chorych na gruźlicę, w 1966 r. otwarto sanatorium dla dorosłych. Od 1979 r. obiekt nosił nazwę „Sanatorium Chorób Płuc i Gruźlicy Staszycówka w Ludwikowie”, od 1996 r. – Szpital Chorób Płuc i Gruźlicy „Staszycówka”, od 1999 r. – Szpital Chorób Płuc i Gruźlicy im. St. Staszica, a od 2002 r. – Wojewódzki Specjalistyczny Szpital Gruźlicy i Chorób Płuc im. St. Staszica w Ludwikowie k. Poznania.
Bez względu na rozmaite zmiany historyczne, Ludwikowo zawsze spełniało swoje zadanie jako uzdrowisko, tak zwany „luftkurort”, ze względu na wyjątkowe walory tamtejszego powietrza.
Porównując położenie Ludwikowa i Poznania, należy zauważyć, iż Poznań leży na Nizinie Wielkopolsko-Kujawskiej, nad środkowym biegiem Warty oraz u jej dopływów: Cybiny, która spiętrzona tworzy Jezioro Maltańskie, Głównej oraz Bogdanki tworzącej jezioro Rusałka i stawy Sołackie.
Śródmiejska część Starego Miasta wraz z przylegającymi doń częściami Jeżyc i Grunwaldu obejmuje głównie mieszkalnictwo wielorodzinne, usługi, drobny przemysł i rzemiosło Wildy i Grunwaldu. Znaczna część tego obszaru posiada gęstą zabudowę 4-5-kondygnacyjną z dużym udziałem budynków ogrzewanych z lokalnych kotłowni, małych kotłowni węglowych lub indywidualnymi piecami węglowymi.
Duża ilość rozproszonych warsztatów rzemieślniczych (lakiernie, galwanizernie i stolarnie) oraz średniej wielkości zakładów przemysłowych oddziaływuje lokalnie na stan zanieczyszczenia powietrza. Natomiast Ludwikowo leży na południowo-zachodnim obrzeżu Wielkopolskiego Parku Narodowego (WPN), w jego otulinie, na zachód od Mosiny (dojazd przez Krosinko ok. 5 km), na północny wschód od rezerwatu „Góry Szwedzkie” i Jeziora Budzyńskiego oraz na północ od jeziora Kociołek.
Zakład leczniczy położony jest na jednym z wyższych w skali Parku wzgórz (113 m n.p.m.), które jest częścią moreny lodowcowej z okresu zlodowacenia bałtyckiego, wśród boru mieszanego, z przewagą sosny.
W folderze wydanym w latach 30-tych XX w. szpital opisuje się w następujący sposób: „Sanatorium „Staszycówka” w Ludwikowie, należące do Okręgowego Związku Kas Chorych w Poznaniu, położone jest na Wyżynie Ludwikowskiej 112 m. n.p.m., w odległości 24 km na południe od Poznania (stacja kolejowa Mosina). Teren sanatoryjny spada łagodnie ku południowi, ku Warcie, od zachodu granicę stanowi stary stuletni bór, wchodzący częściowo w skład rezerwatów kórnickich, częś-ciowo zaś należący do lasów państwowych; ku północy i wschodowi teren sanatoryjny spada gwałtownie i pokryty jest przepięknym starym parkiem z kilkoma malowniczymi wąwozami.
Zabudowania sanatoryjne toną w gęstwinie drzew szpilkowych różnego wieku, w szlachetnych gatunkach. Wyjątkowe piękno krajobrazu ludwikowskiego zjednało mu nazwę „Perły Wielkopolski”.
Otaczające sanatorium lasy ciągną się przez 2 powiaty, tworząc leś-ny obszar blisko 40 000 morgów, stanowiący wspaniałą rezerwę powietrzną dla sanatorium. Teren ściśle sanatoryjny obejmuje około 250 morgów magdeburskich.
Najwybitniejszy „ochroniarz” przyrody, Adam Wodziczko pisał: „Połączony lasami z Puszczykowem teren Ludwikowa to najpiękniejszy zakątek Ziemi Wielkopolskiej. Urozmaicony, pagórkowaty obszar moreny czołowej, liczne jeziora i piękne lasy, bogaty, obfitujący w zabytki przyrody świat roślinny i zwierzęcy”.
Zestawienie stężeń zanieczyszczeń, według obowiązujących norm prawnych, wskazuje jednoznacznie na wyższą jakość powietrza w okolicach Ludwikowa na terenie otuliny WPN, w porównaniu z terenem miasta Poznania. Tak duża różnica w składzie zanieczyszczeń powietrza między omawianymi obszarami jest spowodowana wielusetletnią różnicą w sposobie użytkowania obu terenów. Miasto będące skupiskiem ludzi jest równocześnie miejscem nienaturalnego zagęszczenia przejawów ludzkiej działalności, co ma drastyczny wpływ na stan środowiska, życie i zdrowie jego mieszkańców. Teren Wielkopolskiego Parku Narodowego był terenem wiejskim i leśnym, a od 1945 r. nadano mu rangę Parku Narodowego i stąd objęty jest wieloaspektową ochroną, mającą na celu maksymalne utrzymanie jego naturalnego charakteru.
Godne podkreślenia są własności zdrowotne borów sosnowych. Krzymowska-Kostrowicka podaje, że: „jest to typ zbiorowiska oddziałujący leczniczo na choroby układu oddechowego. Substancje lotne, poza silnym działaniem detoksykacyjnym, obniżają ciśnienie krwi i wpływają tonizująco na układ nerwowy (...). Środowisko borów sosnowych jest w zasadzie wolne od czynników chorobotwórczych, zarówno mikrobiologicznych jak i palinogenicznych (pyłki brzóz i sosen jedynie w nielicznych przypadkach powodują powstanie dolegliwości alergicznych)”.
Niektóre dolegliwości dróg oddechowych zaliczane są do schorzeń cywilizacyjnych, będących wynikiem zmian trybu życia i stanu środowiska. Logiczna wydaje się być więc potrzeba wspomagania nowoczesnej diagnostyki i terapii medycznej zmianą otoczenia na mniej skażone. Te warunki zapewnia położenie Szpitala w Ludwikowie, oferując ponadto korzystny mikroklimat i odmienne od miejskich warunki wypoczynku, będące pochodną typu lokalnego drzewostanu i budowy geomorfologicznej terenu, zauważone już ponad 100 lat temu przez entuzjastów, którzy wybudowali w tym miejscu „luftkurort” na Ludwikowskiej Górze.
Spis treści
W ciągu ostatnich kilku dziesięcioleci znaczenie chorób płuc stale rośnie i nie tylko z powodu zwiększenia się zachorowalności na poszczególne tego typu choroby, ale z powodu zanieczyszczenia środowiska, palenia papierosów.
Światowa Organizacja Zdrowia szacuje, że w roku 2020 palenie tytoniu będzie przyczyną 1 na 10 zgonów.
Koszty świadczenia bezpośredniej opieki leczniczej osobom z chorobami przewlekłymi szacowano w 1990 r. w USA na 425 miliardów dolarów.
W Polsce z powodu chorób płuc przyznaje się około 20 % rent inwalidzkich. Poniżej wymieniono i omówiono te ze wspomnianych chorób, które są najczęstszą przyczyną niezdolności do pracy.
Po raz pierwszy choroba ta została opisana przez francuskiego lekarza René Laënneca. Natomiast terminu „zapalenie oskrzeli” po raz pierwszy użył Badham w 1808 r.
W okresie gwałtownego rozpowszechnienia nałogu palenia tytoniu w XX w. lawinowo rośnie liczba chorych z nieodwracalnym zwężeniem oskrzeli. W 1959 r. na posiedzeniu Sympozjum Fundacji Ciba ustalono definicję przewlekłego zapalenia oskrzeli (PZO) i rozedmy płuc. PZO zdefiniowano jako kaszel ze skąpym odkrztuszaniem, trwający co najmniej 3 miesiące w roku w ciągu 2 kolejnych lat. Natomiast rozedma jest chorobą polegającą na powiększeniu przestrzeni powietrznych położonych obwodowo od oskrzela końcowego, przebiegającą ze zniszczeniem ścian pęcherzyków płucnych bez cech wyraźnego zwłóknienia.
Terminu przewlekła obturacyjna choroba płuc pierwszy użył Burrows, określając ją jako chronic obstructive pulmonery disease. POCHP jest stanem chorobowym, charakteryzującym się obecnością zwężenia dróg oddechowych, spowodowanego przewlekłym zapaleniem oskrzeli lub rozedmą: zwężenie dróg oddechowych jest zazwyczaj postępujące, może mu towarzyszyć nadreaktywność oskrzeli i może być częściowo odwracalne.
W najnowszym badaniu WHO, poświęconym POCHP (GOLD 2002), sformułowano następującą roboczą definicję POCHP: „Jest to choroba charakteryzująca się niecałkowicie odwracalnym ograniczeniem przepływu powietrza przez drogi oskrzelowe. Ograniczenie to jest zwykle postępujące i wiąże się z nieprawidłową odpowiedzią zapalną płuc na szkodliwe pyły lub gazy”.
Pojęcie POCHP jest ściśle powiązane z parametrami spirometrycznymi, co do stopnia ciężkości: I – lekka POCHP, przy której FEV1/FVC < 70%, a FEV1 < 80%; II – umiarkowana POCHP – FEV1/FVC < 70%, a 30% < FEV1 < 80%; III – ciężka POCHP – FEV1/FVC < 70%, a FEV1 < 30%.
Liczba hospitalizacji z powodu POCHP w Polsce wynosi około 120 000 rocznie, a zgony z powodu tej choroby w naszym kraju są 2-krotnie niższe niż w USA i znajdują się na poziomie 170 na 100 000 ludności.
Najważniejszymi czynnikami w etiologii tej choroby są: palenie tytoniu, zanieczyszczenie powietrza, zakażenia, warunki socjalne, niedobór b-antytrypsyny.
Podstawowymi objawami w POCHP są: duszność, kaszel z odkrztuszaniem śluzowej plwociny, która w czasie zakażeń zmienia się w ropną. Duszność narasta powoli w ciągu lat. Równolegle postępuje ograniczenie wydolności fizycznej.
Nasilenie objawów zależy od stopnia zwężenia oskrzeli i zaawansowania rozedmy, ale objawy fizykalne nie zawsze odzwierciedlają stopień upośledzenia wentylacji i wymiany gazowej.
W diagnostyce najczęściej zwraca się uwagę na zaburzenie czynnościowe (spirometria, pletizmografia), RTG klatki piersiowej oraz badania tolerancji wysiłkowej, gazometria.
Leczenie POCHP składa się z wielu etapów. Zaczyna się od leków przeciwzapalnych w okresach zakażeń (antybiotyki, mukolityki); leków rozszerzających oskrzela (adrenolityki, cholinolityki) – chociaż odwracalność w obturacji u tych chorych jest niewielka; kortykosteroidów (opinie są podzielone); następnie tlenoterapia, która przedłuża życie chorych i ratuje je w czasie nasilenia objawów oraz systematyczna rehabilitacja.
Niewątpliwie na równi z POCHP astma oskrzelowa jest częstą przyczyną hospitalizacji, a na jej zwalczanie wydaje się coraz to większe środki finansowe.
Pierwsze wzmianki o astmie datuje się 1500 r. p.n.e. Hipokrates (460-377 r. p.n.e.) w aforyzmach opisuje dokładnie astmatyczny napad duszności.
Ogromnym krokiem w rozwoju diagnostyki astmy było wprowadzenie testów skórnych – zastosowanych przez von Pirgnete, Kocha i Schicka.
Ale czymże jest astma? Podaję za W. Droszczem, iż „Astma jest to zespół chorobowy polegający na napadowym, odwracalnym zwężeniu dróg oddechowych, z nadreaktywnością oskrzeli zawsze w aktywnym i w większości przypadków w nadreaktywnym okresie choroby, którego podłożem są zmiany zapalne drzewa oskrzelowego”.
Podział astmy na atopową i nieatopową czyli na astmę „alergiczną i niealergiczną”, jest najbardziej logiczny. Astma nieatopowa dzieli się na astmę zaostrzoną przez infekcję z nietolerancją niesteroidowych leków przeciwzapalnych, astmę wysiłkową oraz o innej etiologii.
Podział kliniczny określa raczej przebieg astmy, czyli stopnie ciężkości, dzieląc ją na astmę lekką (sporadyczną), umiarkowaną i ciężką – w zależności od częstości napadów duszności i parametrów spirometrycznych (PEF, FEV1).
Częstość występowania duszności w rytmie rocznym przypada wiosną (pyłki roślin), późną jesienią, zimą (pleśnie, roztocza, infekcje). W ciągu dnia duszność występuje częściej w godzinach wieczornych i nocnych, dlatego że nocą spada stężenie kortizolu i adrenaliny w osoczu, natomiast wzrasta histaminy, znamiennie spada % PEF (szczytowy przepływ wydechowy).
Klinicznie napad duszności wygląda następująco (jak go opisuje W. Orłowski): „Napady dychawicy oskrzelowej najczęściej pojawiają się w nocy. Chory budzi się nagle wśród duszności, która zwykle tak wzrasta, iż wreszcie chory po prostu nie może złapać tchu. Odczuwając gwałtowny głód powietrza, chory rzuca się zwykle do okna, otwierając je nawet zimą i opierając się o parapet, by stworzyć punkt oparcia dla głębokich oddechów, stara się pokonać brak tlenu. Na twarzy uwidacznia się ogromny niepokój i trwoga. Szybko dołączają się świsty w klatce piersiowej tak głośne, że słyszy się je nawet w sąsiednim pokoju. Po pewnym czasie oddychanie powoli staje się swobodniejsze, pojawia się kaszel, początkowo z plwociną ciągnącą się, później coraz płynniejszą, sinica maleje, świsty cichną i napad ustępuje”.
Czasami napad duszności nie ustępuje nawet po zastosowaniu tradycyjnego leczenia rozszerzającego oskrzele – wtedy mówimy o stanie astmatycznym.
Leczenie astmy rozpoczyna się od zapobiegania jej powstawaniu: najlepiej, żeby poród dziecka w rodzinie obciążonej alergią odbywał się poza okresem pylenia roślin i rozwoju roztoczy; żeby matka w okresie ciąży i karmienia nie paliła papierosów; dobrze jest przedłużyć okres karmienia piersią; dobrze jest zrezygnować z używania gazu w gospodarstwie domowym i hodowania zwierząt futerkowych; dobrze, jeśli mieszkanie jest urządzone w sposób hipoalergiczny (bez dywanów itp.). W późniejszym okresie dobrze jest unikać kontaktu z czynnikami przyczynowymi, a w przyszłości duże korzyści lecznicze może przynieść odczulanie.
Natomiast w leczeniu farmakologicznym należy uwzględnić:
leki pobudzające receptory adrenergiczne – naturalnym hormonem których jest adrenalina (salbutamol, formeteral, salmeterol i inne),
glikokortykosteroidy (G K S) – w leczeniu astmy spowodowały przełom i pozwoliły na względnie normalne życie tych chorych (hydrocortison, prednizon, dexametazon), zwłaszcza formy do podania we wziewach (budesonid, fluticazon),
teofilinę – jako lek uzupełniający w leczeniu astmy oskrzelowej,
leki przeciwhistaminowe (klemastyna, cetirizina, loratadyna) – tylko przy towarzyszącym alergicznym nieżycie nosa,
w ostatnim ćwierćwieczu pojawiły się leki uzupełniające, do których zalicza się: a) kromony wprowadzone do leczenia w 1965 r. (intal), b) antyleukotrieny (singular, accolate, onon, zyflo).
Zmiany zapalne w płucach najczęściej wywołują bakterie, ale mogą być to także wirusy, grzyby, pasożyty. Liczba leczonych w szpitalach z powodu zapalenia płuc w Polsce waha się w granicach 120 000 rocznie, a liczba zgonów z tego powodu to około 5 000. Nie jest to mało, uwzględniając szybki postęp farmakoterapii i coraz to nowszych antybiotyków stosowanych w leczeniu zapalenia płuc.
Uważa się, że większość zmian wywołują bakterie Streptococcus pneumoniae oraz Haemophylus influenzae. Przyczyną nietypowych zapaleń jest Mycoplazma i Chlamydia, rzadziej Legionella pneumophilia.
Objawy zapalenia występują wśród całkowitego zdrowia, ale są i czynniki sprzyjające jego powstawaniu: starszy wiek, niedożywienie, przewlekłe zapalenia oskrzeli, zmiany marskie po przebytej gruźlicy, zapaleniach płuc itp.
Choroby nowotworowe także sprzyjają powstawaniu zapalenia płuc. Nawet leki stosowane w leczeniu choroby nowotworowej jak i napromienianie mogą doprowadzić do zmian zapalnych w płucach.
Niewątpliwą przyczyną jest też tutaj nałóg palenia tytoniu, urazy i stłuczenia klatki piersiowej, intubacja przy zabiegach chirurgicznych oraz refluks żołądkowo-przełykowy (zwłaszcza w zachłystowym zapaleniu płuc).
W ciągu kilku ostatnich lat nierzadko przyczyną zapalenia płuc jest zespół nabytego upośledzenia odporności (AIDS), wywołany wirusem HIV, w wyniku czego dochodzi do nadkażenia bakteriami, wirusami, grzybami. W roku 2003 mieliśmy do czynienia z groźną postacią zapalenia, wywołaną przez koronawirus z ciężką niewydolnością oddechową i wysoką śmiertelnością (SARS).
Coraz częściej pojawiają się zapalenia płuc w wyniku zakażeń powstałych w szpitalach, wywołane najczęściej przez Klebsiella pneumoniae, Pseudomonas aeruginsa, Escherichia coli, Proteus sp., Enterobaeter sp. – w dużej mierze oporne na wiele tradycyjnych antybiotyków.
Zapalenie płuc zazwyczaj zaczyna się i manifestuje wysoką temperaturą ciała, kaszlem (suchym na początku, męczącym), dusznością, bólami w klatce piersiowej, wykrztuszeniem śluzowo-ropnej wydzieliny. Czasami może wystąpić biegunka, bóle mięśniowe, bóle głowy, a także ostra niewydolność oddechowa.
Obraz kliniczny nasuwa podejrzenie zapalenia płuc. Badaniem potwierdzającym takie rozpoznanie jest RTG klatki piersiowej (z typowym obrazem radiologicznym) oraz leukocytoza wykazana w badaniu morfologicznym krwi, przy podwyższonym OB (opadzie krwinek czerwonych).
W celu określenia prawdopodobnej przyczyny zakażenia, konieczne jest wykonanie bakteriologicznego badania plwociny albo wymazu, jeśli pacjent nie odkrztusza plwociny (w razie konieczności pobiera się popłuczyny metodą bronchoskopową). Wyhodowanie drobnoustroju z pobranego materiału ma zasadnicze znaczenie w doborze antybiotyku, a więc i skuteczności całego leczenia.
W ostatnich czasach w dużych ośrodkach specjalistycznych stosuje się metodę wykrywania cząsteczek DNA za pomocą sondy genetycznej, co pozwala na natychmiastową identyfikację bakterii.
Leczenie prostych niepowikłanych zapaleń płuc rozpoczyna się w warunkach domowych. Empirycznie zakładając, iż pozaszpitalne zapalenie może być wywołane przez Chlamydie, Mycoplazmy, Streptococcus pneumoniae, zaleca się podanie makrolidów: klarytromycyny, roksytromycyny, azytromycyny.
Wobec wzrastającej liczby szczepów Haemophylus influenzae, opornych na ampicylinę, chory powinien otrzymać albo amoksycyclinę z kwasem klawulanowym, ampicylinę z sulbaktanem lub cefalosporyny II generacji.
Chorzy wymagający hospitalizacji powinni otrzymać antybiotyki działające na drobnoustroje wywołujące pozaszpitalne zapalenia płuc: cefalosporyny II, III generacji (cefriakson, cefataksyn) albo a/b z inhibitorem B-laktamazy, co może być zastąpione makrolidem lub skojarzone z makrolidem.
Szybkie zastosowanie leczenia przeciwzapalnego przynosi skutki już w ciągu 1-2 doby: obniża się temperatura ciała, zmniejszają się kaszel, duszność, bóle w klace piersiowej. Ale niekiedy leczenie nie odnosi skutku. Przyczyną mogą być nieskuteczne leki albo pojawienie się płynu w opłucnej (surowiczego, rzadziej ropnego), co wymaga jego usunięcia albo zastosowania drenażu ssącego w przypadku ropniaka opłucnej. Niestosowanie tej metody może doprowadzić do powstania przetoki oskrzelowo-opłucnej i zrostów opłucnych.
W zależności od lokalizacji zmian zapalnych, może dojść do zapalenia osierdzia. Jako powikłanie może wystąpić zapalenie opon mózgowo-rdzeniowych, zapalenie stawów, niewydolność krążenia. Nietypowe zapalenia płuc często mogą także doprowadzić do powstania ropnia płuc (zachłystowe zapalenie płuc), mnogich nacieków z martwicą tkanki płucnej albo wielokomorowego ropnia opłucnej.
Opłucna to cienka błona surowicza pokrywająca płuca na zewnątrz oraz wyścielająca od wewnątrz jamę klatki piersiowej. Każde płuco ma własną opłucną, a każda z nich składa się z dwu blaszek – opłucnej ściennej i opłucnej trzewnej. Łączą się one ze sobą we wnęce płuca i płynnie przechodzą jedna w drugą.
Pojawienie się płynu w jamie opłucnej stanowi zawsze problem diagnostyczny: czy to jest objaw choroby opłucnej, czy objaw towarzyszący chorobie układu oddechowego, czy też jest wynikiem zaburzenia związanego z chorobą innego układu.
Płyn gromadzący się w jamie opłucnej może mieć charakter płynu surowiczego (w zależności od mechanizmu gromadzenia ubogobiałkowego – przesiękowego, albo bogatobiałkowego – wysiękowego), płynu ropnego, krwistego lub chłonkowego. Zwiększenie ilości płynu opłucnowego jest podstawowym objawem występującym w chorobach opłucnej.
Większość objawów klinicznych zależy od ilości nagromadzonego płynu. Jeżeli płynu jest niewiele, to i objawy są nieznaczne. Na pierwszy plan wysuwa się zawsze ból w klatce piersiowej po stronie chorej, nasilający się przy oddychaniu, zmieniający się intensywnie z bólu ostrego na bardziej tępy. Ból pochodzi z podrażnienia opłucnej ściennej, bo opłucna trzewna nie ma unerwienia czuciowego.
Mniej charakterystycznym objawem jest suchy kaszel. Duszność pojawia się w przypadku znacznej ilości płynu uciskającego na płuco, co w sposób znaczący pogarsza warunki wymiany gazowej.
Z badań dodatkowych potwierdzających rozpoznanie zapalenia opłucnej na pierwszy plan wysuwa się badanie RTG klatki piersiowej – wolny płyn w jamie opłucnej układa się zgodnie z siłami grawitacji. Badaniem uzupełniającym jest badanie ultrasonograficzne. Umożliwia ono dokładną ocenę grubości warstw płynu, głębokość na której on się znajduje i czy jest otorbiony.
Płyn w jamie opłucnej najczęściej towarzyszy zapaleniu płuc, ale może pojawić się też przy ropniu płuca, zakażonych rozstrzeniach oskrzeli.
Najczęstszą przyczyną wysiękowego zapalenia opłucnej są: Streptococcus pneumoniae, Streptococcus pyogenes: Haemophylus influenzae, Klebsiella. Leczenie polega na opróżnieniu jamy opłucnej od płynu, czasami wymagany jest drenaż i podanie leków doopłucnowo oraz podanie antybiotyków dożylnie, zgodnie z lekowrażliwością.
W ropnym zapaleniu opłucnej wymagane jest założenie drenażu ssącego oraz podanie dożylnie 2 antybiotyków o szerokim zakresie działania oraz dobrej penetracji do jam ciała. Im dłużej utrzymuje się płyn ropny w jamie opłucnej, tym większe prawdopodobieństwo powstania zrostów i wytworzenia się wielu przestrzeni płynowych, co niezwykle utrudnia leczenie i rehabilitację tych chorych.
Trzeba brać pod uwagę jeszcze fakt, że przyczyną wysięku w jamie opłucnej może być gruźlica, co świadczy o szerzeniu się procesu swoi-stego. A jeżeli do opłucnej przebije się serowate ognisko zawierające prątki, to może dojść do ropniaka opłucnej. W tym przypadku, jak również przy bakteryjnym ropnym zapaleniu opłucnej, zakłada się drenaż, ale doopłucnowo. Ogólnie podaje się leki przeciwgruźlicze: izoniazyd, rifampicynę, przy ciężkim przebiegu – steroidy.
Obecnie najczęstszą przyczyną wysięku jamy opłucnej są nowotwory płuc lub narządów sąsiednich. Jako choroba wtórna, towarzysząca bakteryjnemu lub wirusowemu zapaleniu płuc, urazom klatki piersiowej, chorobie reumatycznej – występuje suche zapalenie opłucnej, które charakteryzuje się nagle pojawiającym się kłującym bólem w klatce piersiowej, nasilającym się przy kaszlu i oddychaniu. Ból może promieniować do jamy brzusznej lub ramienia. Na RTG klatki piersiowej może się pojawić pogrubienie opłucnej przy ścianie klatki piersiowej. Leczenie choroby podstawowej prowadzi do wyleczenia także i choroby wtórnej.
Czasami przy urazie klatki piersiowej albo pęknięciu pęcherza rozedmowego w płucu do jamy opłucnej przedostaje się powietrze, a tym samym znosi się ujemne ciśnienie panujące w niej. Proces ten nosi nazwę odmy opłucnej. Po stronie odmy płuco zapada się i częściowo lub całkowicie jest wykluczone z funkcji oddychania, a powietrze, uciskając na duże naczynia, powoduje zachwianie krążenia. Wszystko to jest przyczyną znacznego zmniejszenia stosunku wentylacji do perfuzji i wystąpienia hipoksji oraz groźnej dla życia kwasicy.
Rozróżnia się odmę opłucnową bez nadciśnienia i z nadciśnieniem albo inaczej odmę wentylową (zastawkową) – gdy powietrze dostaje się do jamy opłucnej podczas wdechu, a przy wydechu drogą ewakuacji jest ona zamknięta. Ciśnienie w jamie opłucnej rośnie przy każdym wdechu – jest to najbardziej niebezpieczny mechanizm, wymagający natychmiastowego wyrównania ciśnienia w niej po stronie chorej.
Kliniczne objawy pojawiają się nagle w postaci narastającej duszności, suchego kaszlu, niepokoju bądź lęku o swoje życie, sinicy. Oddechy są płytkie, przyspieszone, występuje znaczne przyspieszenie pracy serca.
W rozpoznaniu decydujące jest RTG klatki piersiowej, gdzie stwierdza się zapadnięcie płuca.
Leczenie jest skierowane na nakłucie opłucnej, aspirację powietrza albo założenie drenażu ssącego, leki uspokajające.
W ciężkich urazach klatki piersiowej konieczna jest interwencja chirurgiczna.
W ostatniej dekadzie znacznie poprawiła się diagnostyka nowotworów płuc, a co za tym idzie – statystyczne zwiększenie przypadków zachorowania na tę groźną chorobę. Na częstszą zapadalność na raka płuc złożyło się zwiększenie liczby osób nałogowo palących tytoń, co poskutkowało 4-krotnym wzrostem występowania raka płuc w Polsce w ciągu ostatnich 20 lat. Corocznie z powodu raka płuc umiera około 20 000 osób.
Nowotwory płuc charakteryzują się dużym zróżnicowaniem, dotyczącym pochodzenia tkankowego, budowy komórkowej, biologii, co rzutuje na ich przebieg kliniczny.
Ogólnie nowotwory płuc dzielą się na łagodne i złośliwe. Łagodne występują znacznie rzadziej od złośliwych. Do łagodnych zaliczamy: brodawczaki, chrzęstniaki, gruczolaki, mięśniaki, naczyniaki, nerwiakowłókniaki, włókniaki.
Objawy kliniczne i obraz radiologiczny łagodnych nowotworów mogą być zbliżone do objawów występujących przy złośliwych nowotworach. Jak każda zmiana wzrastająca wewnątrzoskrzelowo, prowadzą do zmniejszenia światła oskrzela i powodują objawy typowe do obturacji dróg oddechowych, takie jak: kaszel, duszność, krwioplucie oraz nawracające zmiany zapalne.
Leczeniem z wyboru łagodnych nowotworów płuc jest ich resekcja, czyli podstawową metodą jest leczenie chirurgiczne, a rokowanie w większości przypadków jest pomyślne.
Do nowotworów złośliwych zaliczamy rak płuca: płaskonabłonkowy, drobnokomórkowy, gruczolakorak, wielkokomórkowy i gruczołowo-płaskonabłonkowy; rak śluzowo-naskórkowy, mięsak płuc i międzybłoniak opłucnej.
Rak płuca jest jednym z najczęściej występujących nowotworów złośliwych. Najwyższa zachorowalność występuje w Anglii, Finlandii i Holandii. Polska należy do krajów o średniej zapadalności na raka płuc, wynoszącej odpowiednio 50/100 000 mężczyzn i 8/100 000 kobiet. Najwyższą zachorowalność notuje się u mężczyzn powyżej 50 roku życia, a do najważniejszych czynników odgrywających w niej rolę zalicza się palenie papierosów.
Ryzyko rozwoju raka płuca u mężczyzny palącego około 30 papierosów dziennie przez okres dłuższy niż 10 lat jest około 10-krotnie większe niż u osoby nigdy niepalącej. Wypalanie powyżej 40 papierosów dziennie zwiększa to ryzyko do 60 razy.
Najważniejszymi czynnikami rakotwórczymi są: benzopiren, dwubenzopiren, benzoantracen, metylochryzen – są one produktami niecałkowitego spalania tytoniu.
Wśród czynników zawodowych powodujących raka płuca trzeba wymienić pracę przy azbeście, przetwórstwie chromu, niklu i arsenu oraz w kopalniach rud radioaktywnych.
Rak płuca może się także rozwijać na podłożu istniejących w nim zmian bliznowatych pogruźliczych.
Podstępność raka płuca polega na jego długim bezobjawowym rozwoju. Na początku pojawiają się objawy ze strony układu oddechowego: kaszel, bóle w klatce piersiowej (często mylnie traktuje się je jako objawy nieżytu oskrzeli), bóle o charakterze neuralgii ramiennej (co po 50 roku życia przyjmuje się za bóle reumatyczne). Objawem, którego nikt nie lekceważy, jest krwioplucie (występuje u około 8% chorych), mające postać plwociny z domieszką krwi. Częste nawroty zakażeń płuc mogą być objawem nie tylko obniżonej odporności, ale i wewnątrz-oskrzelowego umiejscowienia guza. W wyniku jego ucisku następuje porażenie nerwu krtaniowego wstecznego co objawia się chrypką. Innym objawem zajęcia śródpiersia przez guz jest porażenie nerwu przeponowego.
Przy nacieczeniu przez nowotwór osierdzia może się pojawić płyn wysiękowy w worku osierdziowym, co w zaawansowanym przypadku może doprowadzić do tamponady serca.
Przy zajęciu opłucnej pojawia się płyn krwisty w jamach opłucnych.
W zaawansowanych stanach dochodzi do powstania objawów ogólnych, takich jak: ubytek masy ciała, ogólne osłabienie, brak łaknienia, mięsowstręt, niewyjaśnione stany gorączkowe – co może świadczyć o niepomyślnym przebiegu choroby.
Równolegle notuje się objawy paranowotworowe: przerostową osteoartropatię płucną (bóle, obrzęki stawowe), zaburzenia neurologiczne (neuroencefalopatia), zmiany skórne (dermatomyosity, sklerodermia itd.), nadkrzepliwość krwi.
W ustaleniu rozpoznania oprócz RTG klaki piersiowej, tomografii komputerowej, zasadnicze znacznie odgrywa bronchofiberoskopia wzbogacona o badanie cytologiczne jak i histopatologiczne, jeżeli zmiana nowotworowa znajduje się w świetle oskrzela. Przy obwodowym położeniu guza wymagana jest cienkoigłowa biopsja pod kontrolą tomografii komputerowej.
W leczeniu raka płuca stosuje się 3 główne metody lub ich skojarzenie: leczenie chirurgiczne, radioterapię, chemioterapię.
Zasadniczym podziałem jest podział na leczenie w rakach drobnokomórkowych i niedrobnokomórkowych. W tych ostatnich, do których można zaliczyć raka płaskonabłonkowego, gruczołowatego i wielkokomórkowego – zasadniczym leczeniem jest leczenie chirurgiczne. W przy-padkach zaawansowanych (III A) przed leczeniem chirurgicznym stosuje się tzw. neoadjuwantową chemio- albo radioterapię, co poprawia skuteczność leczenia.
U chorych nie kwalifikujących się do leczenia chirurgicznego stosowane jest leczenie promieniami jonizującymi o założeniu radykalnym.
Podstawowym leczeniem w przypadku raka drobnokomórkowego jest chemioterapia, co pozwala uzyskać wydłużenie przeżycia aż u 90% chorych.
Radioterapia w leczeniu raka drobnokomórkowego jako jedyna metoda nie znajduje zastosowania. Natomiast znajduje ona duże zastosowanie w profilaktyce przerzutów do mózgu.
Jednym z najbardziej rozpowszechnionych zakażeń na świecie jest zakażenie prątkiem gruźlicy. Światowa Organizacja Zdrowia szacuje, iż w latach 90. wśród 5,4 mld ludności zamieszkującej kulę ziemską około 1,7 mld (tj.1/3) to ludzie zakażeni prątkiem gruźlicy. Spośród nich około 5-8% zachoruje w ciągu swojego życia na czynną gruźlicę, a połowa będzie stanowiła źródło dalszych zakażeń prątkiem.
Liczba nowych zachorowań na gruźlicę w ciągu roku na świecie wynosi około 7-9 mln (w tym potwierdzonych bakteriologicznie 3,5-4,5 mln), natomiast liczba chorych na gruźlicę (tj. nowych zachorowań + choroby z lat poprzednich) wynosi około 15-18 mln. W ciągu roku umiera na gruźlicę około 3 mln osób, z czego 95% w krajach rozwijających się.
W Polsce zachorowalność na gruźlicę występuje na poziomie 34,3/100 tys. ludności i nie zmienia się w sposób znaczący. Dla porównania w Europie Zachodniej średnia zachorowalność to 23/100 tys. ludności.
Niezbędnym warunkiem zachorowania na gruźlicę jest zakażenie się zjadliwym prątkiem gruźlicy, ale nie każde zakażenie prowadzi do zachorowania i jest uzależnione od poziomu odporności ustroju. W normalnych warunkach zachoruje nie więcej niż 10% osób.
W wyniku kontaktu z chorym prątkującym dochodzi do zakażenia gruźlicą podczas kaszlu, rozmowy, kichania, śpiewu – kiedy to chory wydziela na zewnątrz drobne kropelki plwociny (cząsteczki o wielkości 1-5 mikronów), a w każdej z nich znajduje się 2-3 bakterii. Najmniejsze z cząsteczek przedostają się aż do pęcherzyków płucnych.
Niestety, zakażenie prątkiem gruźlicy najczęściej przebiega bezobjawowo. Jedynym skutkiem zakażenia jest wiraż odczynu tuberkulinowego z ujemnego na dodatni. Do zachorowania na gruźlicę usposabiają sytuacje z obniżoną odpornością w rezultacie: nowotworów układu chłonnego, chorób metabolicznych, stosowania leków immunosupresyjnych, a także sytuacje związane z niedożywieniem i stresem. Pierwszym objawem gruźlicy jest powstanie zespołu pierwotnego (po kontakcie z chorym wydalającym prątki) – drobnego nacieku tkanki płucnej z powiększeniem węzłów chłonnych we wnękach. W części przypadków dochodzi do zwapnienia ogniska i węzłów chłonnych, a zmiany na RTG klatki piersiowej świadczą o przebytym zakażeniu prątkiem gruźlicy.
Gruzełki gruźlicze, powstałe w przebiegu pierwotnego zakażenia, pozostają nieaktywne przez całe życie. Z czasem jednak może nastąpić ich reaktywacja i w zależności od miejscowego stanu odporności może dojść do ograniczonych rozsiewów lub gwałtownego szerzenia się gruźlicy drogami oskrzelowymi oraz powstania serowatego zapalenia płuc.
Około 3% przypadków gruźlicy wykrywanych jest przypadkowo, w czasie badań małoobrazkowych.
Najczęstszym objawem ogólnym gruźlicy są stany podgorączkowe i gorączkowe, temperatura ciała wzrasta po południu i opada w ciągu nocy, co wiąże się z występowaniem potów. Kolejnym objawem jest osłabienie i utrata masy ciała. Częstym miejscowym objawem gruźlicy płuc jest kaszel – w początkowej fazie suchy, następnie z wykrztuszaniem śluzowej i ropnej wydzieliny. Może także występować krwioplucie. Chorzy na gruźlicę mogą skarżyć się na bóle w klatce piersiowej – zwłaszcza przy kaszlu i głębokim oddychaniu, co świadczy o wciągnięciu w proces chorobowy opłucnej.
W późnej fazie choroby może pojawić się duszność. Bardzo nasilona przy wysiękowym zapaleniu opłucnej na tle gruźliczym i prosówce gruźliczej.
Rozpoznanie potwierdzają: dodatni odczyn tuberkulinowy, przyspieszone opadanie krwinek czerwonych (OB), naciekowe zmiany na RTG klatki piersiowej, wyhodowanie z plwociny prątków gruźlicy (ew. z popłuczyn oskrzelowych – BAL, przy bronchoskopii), a w przypadku materiału skąpoprątkowego – dodatni wynik na obecność prątków metodą BACTEC.
Jeżeli leczenie nie rozpocznie się w odpowiednim czasie, dochodzi do groźnych powikłań, między innymi do odmy opłucnej, ropniaka opłucnej, krwotoków płucnych, zwłóknienia opłucnej, towarzyszącego grzybicy płuc. Leczenie gruźlicy jest bardzo skuteczne, choć nie zawsze proste. Jest ono na pewno bardziej skomplikowane niż innych chorób bakteryjnych ze względu na szczególne cechy prątków, takie jak wolne tempo wzrostu, zdolność do zatrzymania metabolizmu i przejścia w stan uśpienia przez wiele lat oraz łatwość powstawania oporności na leki stosowane w monoterapii.
Najbardziej skutecznymi lekami w terapii gruźlicy są: rifampicyna (RMP) działająca na wszystkie typy prątków, izoniazyd (INA) – działający na prątki wewnątrz- i zewnątrzkomórkowo. Te dwa leki stosowane razem zapobiegają rozwojowi lekooporności.
Pyrazynamid (PZA) działa bakteriobójczo na prątki żyjące wewnątrz makrofagów, a streptomycyna (SM) i inne aminoglikozydy działają bakteriobójczo tylko na prątki namnażające się zewnątrzkomórkowo. Pozostałe leki przeciwprątkowe działają bakteriostatycznie.
Standardowe leczenie gruźlicy polega na podawaniu czterech leków: rifampicyny, izoniazydu, pyrazynamidu i streptomycyny lub etambutolu. (EMB).
Czasami schemat leczenia trzeba modyfikować w zależności od nietolerancji chorego wobec niektórych leków i zastępowania ich innymi.
Czas leczenia zazwyczaj (przy braku powikłań i bez występowania oporności na niektóre leki) trwa 6 miesięcy: 2 miesiące intensywnego leczenia i 4 miesiące kontynuacji leczenia podtrzymującego.
Najlepszym dowodem na skuteczność leczenia jest zaprzestanie prątkowania, zmniejszenie występowania objawów i resorpcja zmian w obrazie radiologicznym w czasie leczenia przeciwprątkowego.
Śródmiąższ jest to anatomiczna przestrzeń pomiędzy komórkami nabłonkowymi wyścielającymi pęcherzyki płucne a błoną podstawną i komórkami śródbłonka naczyń włosowatych. W związku z tym do chorób śródmiąższowych zalicza się zarówno te, które toczą się w ścianach pęcherzyków, jak i w obrębie oskrzelików końcowych oraz w otaczającej tkance łącznej.
W klasyfikacji chorób śródmiąższowych należy wymienić:
choroby tkanki łącznej (sklerodermia),
reakcje polekowe,
choroby zawodowe – pylice (krzemica, azbestoza i inne),
zewnątrzpochodne alergiczne zapalenia pęcherzyków płucnych (płuco rolnika, hodowcy ptaków i inne),
pierwotne: sarkoidoza, histiocytoza, amyloidoza i inne,
uwarunkowane genetycznie: stwardnienie guzowate i inne,
samoistne zwłóknienia płuc: ostre, zwykłe, złuszczające i inne.
Częstość występowania tychże chorób w Polsce ocenia się na 30/100 000 osób rocznie. Około 3000 chorych rocznie umiera z powodu choroby śródmiąższowej płuc.
Przyczyna większości tych chorób jest nieznana. Uszkodzenie komórek nabłonka i przerwanie ciągłości błony podstawnej jest niezbędnym warunkiem uruchomienia procesu włóknienia.
Wśród objawów klinicznych notuje się dużą różnorodność. Część chorych zgłasza się z powodu przypadkowego stwierdzenia zmian w obrazie radiologicznym (sarkoidoza). U części chorych stwierdza się objawy przewlekłego zapalenia płuc. Niekiedy pierwszym objawem jest odma samoistna (histiocytoza x). Podwyższona ciepłota ciała jest rzadkością. Natomiast znacznie częściej pojawiają się bóle stawowe. Jednym z najważniejszych objawów chorób śródmiąższowych płuc jest duszność na początku wysiłkowa, a następnie spoczynkowa, narastająca przez wiele miesięcy. Kaszel suchy towarzyszy prawie wszystkim chorobom śródmiąższowym płuc. Rzadko natomiast można spotkać się tutaj z bólem opłucnowym i krwiopluciem.
Z dodatkowych badań pomocnych w ustaleniu rozpoznania można wymienić: leukocytozę, eozynofilię, podwyższenie enzymu konwertującego angiotenzynę (ACE) i obecność przeciwciał przeciwjądrowych oraz krioglobulin. Bardzo ważną rolę odgrywa badanie czynnościowe układu oddechowego, zwłaszcza w ocenie zawansowania choroby.
W stadiach mniej zaawansowanych chorób śródmiąższowych płuc zmiany dotyczą wyłącznie przepływów w drobnych oskrzelach, natomiast w bardziej zaawansowanych pojawiają się zmiany obturacyjne, ale są one odwracalne po zastosowaniu środka rozkurczowego. Jednak zasadniczym badaniem jest badanie radiologiczne klatki piersiowej.
Najczęściej występującą spośród chorób śródmiąższowych płuc jest sarkoidoza, która jest uogólnioną chorobą ziarniniakową o nieznanej etiologii, najczęściej objawiającą się powiększeniem węzłów chłonnych we wnękach płucnych, naciekami w płucach, a także zajęciem innych narządów, np. skóry czy narządu wzroku. Zapadalność na nią wynosi od 10/100 000 w Polsce do 64/100 000 w Szwecji i dotyczy głównie młodych osób, ze szczytem zachorowań przypadającym w przedziale wieku 20-29 rok życia. Na genetyczne uwarunkowanie choroby wskazuje jej rodzinne występowanie.
Sarkoidoza może przebiegać bezobjawowo lub z objawami ogólnymi, które pojawiają się u 30% chorych i polegają na stopniowo narastającym uczuciu osłabienia, podwyższeniu temperatury ciała i utracie masy ciała. Typowy jest ujemny odczyn tuberkulinowy jako jeden z objawów zmniejszonej reaktywności limfocytów na obwodzie.
Zmiany skórne występują pod postacią rumienia guzowatego na kończynach dolnych u 25% chorych.
Tylko 20-50% chorych na sarkoidozę ma objawy ze strony układu oddechowego: suchy kaszel, duszność, nieprawidłowy obraz RTG. Zmiany w RTG dotyczą policyklicznie powiększonych węzłów chłonnych wnęk oraz naciekowych zaciemnień miąższu. W badaniu spirometrycznym występują zaburzenia wentylacji typu restrykcyjnego, zmniejszenie podatności płuc i pojemności dyfuzyjnej. W późnej fazie choroby może rozwinąć się niewydolność oddechowa i serce płucne.
Ziarniniaki sarkoidalne wykryto w węzłach chłonnych jamy brzusznej, wątrobie, sercu.
Przyczynowe leczenie sarkoidozy nie istnieje. W ostrej fazie z objawami kostno-stawowymi i rumieniem guzowatym stosuje się niesterydowe leki przeciwzapalne. W postaci płucnej sarkoidozy w razie braku poprawy przez ponad pół roku progresji zmian radiologicznych oraz pogorszenia czynności wentylacyjnej płuc, wskazane jest podjęcie leczenia
encortonem w dawkach 20-40 mg/d przez 3 miesiące, potem przy uzyskaniu poprawy – kontynuacja leczenia do 12 miesięcy w dawkach 5-15 mg/d. Przy braku skuteczności stosowane są leki cytostatyczne: metotrexat, azatiopryna, cyklofosfamid.
W I stadium sarkoidoza ulega samoistnej regresji w 60-80% w okresie 1-2 lat.
W II stadium remisja występuje u 40-70% chorych, w III – 10-20%, w IV nie obserwuje się samoistnych remisji.
Znaczenie rehabilitacji pneumologicznej w ciągu ostatnich dziesięcioleci wzrosło w sposób znaczący, w związku ze stale rosnącą liczbą chorych na przewlekłe choroby płuc oraz z potrzeby zapewnienia tym chorym jak najlepszej opieki. Podstawowe korzyści wynikające z tego systemu są następujące: zmniejszenie nasilenia objawów chorobowych, poprawa jakości życia, zwiększenie tolerancji wysiłku, niezależność w codziennych czynnościach życiowych oraz mniejsze uzależnienie od pomocy medycznej.
Na początku rehabilitacja dotyczyła tylko przewlekłego zapalenia oskrzeli, rozedmy – innymi słowy stanów związanych z chorobą obturacyjną płuc. Ale później w programy rehabilitacji zostały włączone i inne choroby, m.in. astma oskrzelowa, niedobór n-antytrypsyny, mukowiscydoza, nadciśnienie płucne, rak płuca, zabiegi torakochirurgiczne w okresie przed- i pooperacyjnym oraz inne.
Przez pojęcie usprawniania ruchowego w chorobach płuc rozumie się badanie i edukację chorego, postępowanie fizjoterapeutyczne, oddziaływanie psychospołeczne oraz obserwację i monitorowanie. Kompleksowe podejście niewątpliwie musi uwzględniać także problemy prewencji.
Podstawowym warunkiem skuteczności rehabilitacji jest zrozumienie przez chorego i jego rodzinę przesłanek przemawiających za jej stosowaniem. Bez zrozumienia tego celu rehabilitacja staje się sporadycznym i wymuszonym obowiązkiem.
Definicja rehabilitacji pneumologicznej określona została w 1994 r. przez Narodowy Instytut Zdrowia w USA i brzmi następująco: „Rehabilitacja pneumologiczna jest to wielowymiarowy zakres usług dla chorych na choroby układu oddechowego i ich rodzin, realizowany zwykle przez wielospecjalistyczny zespół specjalistów, mających na celu osiągnięcie i utrzymanie maksymalnego dla chorego poziomu niezależności i aktywności w społeczeństwie”.
Stworzenie szeroko pojętej rehabilitacji pneumologicznej bardzo korzystnie wpływa nie tylko na stan zdrowia: poprawia jakość życia, zmniejsza nasilenie objawów chorobowych, zmniejsza niepokój i objawy depresji, wpływa na zwiększenie tolerancji wysiłku fizycznego, a także poprawia skutki społeczne choroby, mianowicie – zmniejsza liczbę hospitalizacji i zapotrzebowanie na specjalistyczną pomoc medyczną, przedłuża czas przeżycia u niektórych chorych, a nieraz pozwala na powrót do pracy niektórych pacjentów.
Kompleksowa rehabilitacja to nie tylko usprawnianie już chorych ludzi, ale i wczesne wykrywanie kolejnych chorych poprzez badania przesiewowe, w celu niedopuszczenia do stanu, w którym lekarz jest już bezsilny. Ważnym elementem są kryteria doboru pacjentów oraz programy dostosowane do indywidualnych potrzeb chorego, w których uwzględniana ma być edukacja chorego, znaczenie oddziaływania psychospołecznego i konieczność monitorowania przez dłuższy okres.
Straty, które ponosi gospodarka każdego kraju w związku z chorobami płuc, są ogromne. W Stanach Zjednoczonych straty bezpośrednie wyniosły w 1996 r. 33,4 mld dolarów w postaci bezpośrednich kosztów opieki medycznej i 51 mld – kosztów pośrednich. Wydatki na opiekę nad chorymi na POCHP wyniosły 23,5 mld, na astmę 12,4 mld (danych porównywalnych w Polsce – brak).
Wczesne wykrywanie i prewencja są bardzo istotne we wszystkich chorobach płuc, bo zmniejszają koszty leczenia, koszty opieki, kalectwo oraz napawają optymizmem co do rezultatów leczenia. Prostym rozwiązaniem wydaje się być wykonanie przy każdej nadarzającej się ku temu okazji zwykłej spirometrii z prostą oceną VC i FEV1, tak jak mierzy się temperaturę ciała albo ciśnienie krwi lub robi się EKG czy RTG klatki piersiowej.
Początkiem rehabilitacji jest prewencja, czyli programy profilaktyczne skierowane na już istniejące czynniki ryzyka (zaprzestanie palenia tytoniu jako walka z nałogiem uzależnienia od nikotyny).
Każdy pacjent przystępujący do programu rehabilitacji pneumologicznej musi mieć wyznaczone cele, do których ma dążyć z pomocą zespołu rehabilitacyjnego. Należą do nich: poprawa wzoru oddechowego (szkoła prawidłowego oddychania), większa aktywność fizyczna i poprawa przez to jakości życia, zwiększenie siły i wytrzymałości. Nie tylko poprawa zdolności do wykonywania codziennych czynności życiowych, ale i możliwości realizacji swojego hobby, możliwość podróżowania, zmniejszenie niepokoju, zapobieganie zaostrzeniom objawów choroby i hospitalizacjom, powrót do pracy, a co najważniejsze – niezależność i wiara w siebie.
Trzeba pamiętać, iż rehabilitacja pneumologiczna zawsze opiera się na indywidualnie dobranym do konkretnego pacjenta programie. Nie jest on dla pacjenta jakimś ekstradodatkiem do leczenia farmakologicznego, a tylko niezbędnym elementem, zastosowanym w sytuacji konieczności niesienia jak największej pomocy choremu człowiekowi.
Niewątpliwie ogromnym problemem dla chorego jest radzenie sobie z przewlekłą chorobą płuc. Życie w ciągłym stresie i obawie o swoje życie podczas napadu duszności jest niewyobrażalnym przeżyciem. Szybko udzielona pomoc, podane leki łagodzące przebieg tej choroby niestety nie wpływają na tak zwaną pamięć emocjonalną (życie i funkcjonowanie w poczuciu zagrożenia). Stres doprowadzony do potęgi paniki też może wywołać skrajne objawy chorobowe, komplikując w sposób znaczny przebieg choroby. Natomiast pomoc psychologiczna dostępna w Specjalistycznym Szpitalu Chorób Płuc ułatwia proces adaptacji poprzez pobudzenie zachowań ukierunkowanych na proces zmniejszenia i hamowania negatywnych emocji oraz tworzenie wspierającego środowiska społecznego.
Na początku choroby sam chory jest jej często nieświadom, a tym bardziej stanu jej zaawansowania. Czasami nawet stara się tłumić emocje i niepokoje związane z chorobą, ale wraz z jej postępem większość chorych doświadcza strachu i lęku, związanych z występującymi albo przewidywalnymi epizodami duszności. Z kolei niepokój i pobudzenie wzmaga duszności i w ten sposób powstaje błędne koło. Wynikiem tego jest coraz to większy bezruch, obniżenie wydolności fizycznej i oddechowej, a w rezultacie – inwalidztwo.
Frustracja spowodowana złym stanem zdrowia i niezdolnością do wykonywania wielu prostych czynności prowadzi do rozdrażnienia, pesymizmu i wywołuje agresję w stosunku do innych ludzi. W późnych stadiach choroby dochodzi do uczucia rozpaczy i nieradzenia sobie z chorobą. Pojawiają się bezsenność, zaburzenia koncentracji i osłabienie pamięci, myśli samobójcze i brak chęci życia, czyli zestaw objawów klinicznych, który nazywamy depresją. Dotyka ona od 51 do 74% chorych.
Na ogół rzecz biorąc, przyczyny doprowadzające do stałego stresu w chorobach płuc można podzielić na medyczne i psychospołeczne. Do medycznych zaliczamy: duszność, niepożądane działanie leków, zaburzenia wydolności fizycznej (spowodowane przebiegiem choroby, lekami, starzeniem się), zaburzenia czynności poznawczych (koncentracja, pamięć), współistniejące choroby (wieńcowa, zapalenie stawów), zaburzenia snu, depresję, hipoksemię. Do psychospołecznych przyczyn zaliczamy: obawę przed zagrożeniem śmiercią, zmianę roli społecznej, zaburzenia seksualne, oczekiwania rodziny i reakcje ze strony innych osób, zakłopotanie w miejscach publicznych (stała tlenoterapia), utratę pracy –dochodów, obwinianie innych osób, brak widocznych objawów choroby.
Radzenie sobie z takim pacjentem to nie tylko problem klinicznego psychologa, a całego zespołu rehabilitacyjnego, tj.: lekarza, pielęgniarki, rehabilitanta i psychologa – praktyków.
Dzięki umiejętności aktywnego słuchania, praktyk potrafi przekazać choremu prawdziwe współczucie z powodu jego stanu. Umiejętność ta polega na: odpowiednim kontakcie wzrokowym; parafrazowaniu i podsumowywaniu wypowiedzi chorych, zadawaniu pytań pozwalających wyjaśnić istotną kwestię; przyjmowaniu łagodnego, wolnego od osądu podejścia do niekonsekwencji pomiędzy stwierdzeniami wypowiadanymi przez chorego a jego zachowaniem.
Postępowanie polega na indywidualnych spotkaniach z chorym lub spotkaniach grupowych, zależnie od nasilenia zaburzeń emocjonalnych i możliwości leczenia. Porady polegają na zajęciach dotyczących określonego problemu (radzenie sobie ze stresem) lub są prowadzone w ramach innych zajęć rehabilitacyjnych (nauka właściwego sposobu oddychania).
Dodatkowo pomoc w rozwiązywaniu problemów powinna pochodzić od członków rodziny, przyjaciół chorego. Szczególne znaczenie mają rozmowy i zajęcia polegające na rozwijaniu różnego rodzaju umiejętności, które pomogą członkom rodziny zapewnić choremu odpowiednią pomoc bez uzależniania go od niej.
Szkolenie na temat radzenia sobie ze stresem obejmuje przedstawienie łatwego do zrozumienia modelu stresu oraz jego wpływu na umysł i ciało. Chorych uczy się rozpoznawania wczesnych objawów ostrzegawczych – na przykład: niepokoju, duszności, napięcia mięśniowego – i stosowania różnych metod walki ze stresem (relaksacja mięśni, trening autogenny, joga).
W ciężkich zaburzeniach emocjonalnych stosuje się środki farmakologiczne zmniejszające lęk, takie jak: diazepan, hydroksyzynę, lorazepan, oxazepan. Natomiast w przypadku depresji jednobiegunowej wymagane są już leki z grupy trójcyklicznych leków przeciwdepresyjnych oraz selektywnych inhibitorów wychwytu serotoniny (amitryptylina, imipramina, sertralina, trarodon).
Początkowo metody oddziaływania na chorego skupiają się na umiejętności radzenia sobie z nową chorobą, a w kolejnym etapie nacisk jest położony na zapobieganie nawrotom, ułatwiające długotrwałą zmianę zachowania chorego: między innymi poprawę zrozumienia przez chorego i utożsamianie się z każdym elementem programu leczenia; rozwój zdolności chorego do wykrywania sytuacji, które sprzyjają wystąpieniu u niego nawrotu choroby; nauczenie chorego niezależnego rozwiązywania problemów w codziennym życiu; zachęcenie chorego i zaangażowanie jego rodziny w zorganizowanie formy wsparcia społecznego (kluby, programy ćwiczeń) – innymi słowy przeprowadzenie modyfikacji stylu życia chorego na stałe.
Na początku rehabilitacja pneumologiczna była zarezerwowana jedynie dla chorych na POCHP albo dla innych schorzeń płuc ze znacznym upośledzeniem czynności oddechowych i było to pojęcie błędne. Program rehabilitacji pneumologicznej może i musi być dostosowany do potrzeb każdego chorego z chorobą płuc, bez względu na wiek, zaawansowanie choroby, prognozy co do przebiegu. Natomiast niewątpliwie można sprecyzować wskazania do przeprowadzenia rehabilitacji pneumologicznej do chorób przebiegających z obturacją oskrzeli, przebiegających bez obturacji i innych.
Do grupy chorób obturacyjnych można odnieść: szeroko pojętą przewlekłą obturacyjną chorobę płuc (POCHP, przewlekłe zapalenie oskrzeli, rozedmę), astmę oskrzelową, mukowiscydozę, zarostowe zapalenie oskrzelików.
Do grupy chorób bez obturacji należy odnieść choroby opłucnej, choroby śródmiąższowe płuc, sarkoidozę, zwłóknienie samoistne, zwłóknienie reumatoidalne (kolagenozy), choroby ściany klatki piersiowej (kyfoskoliozy), choroby nerwowo-mięśniowe (Parkinsona, stwardnienie rozsiane).
Do innych chorób można zaliczyć: gruźlicę płuc, rak płuca, stan po zabiegach torakochirurgicznych, otyłość, zespół bezdechu sennego.
Podstawowym kryterium kwalifikacji chorego do rehabilitacji jest stopień upośledzenia czynności płuc (duszność, znacznie obniżony FEV1, powikłania). Następnymi kryteriami są: obniżenie wydolności fizycznej, zdolności wykonywania czynności codziennych, zwiększenie zapotrzebowania na usługi medyczne, pogorszenie jakości życia, zmniejszenie zdolności do wykonywania zawodu, zaburzenia psychospołeczne (depresja).
Głównym problemem przy doborze pacjentów do rehabilitacji jest kwestia palenia papierosów. Wymagane jest bowiem bezwzględne rzucenie palenia. Chorzy przystępujący do rehabilitacji pneumologicznej koniecznie muszą rozpocząć ćwiczenia w warunkach szpitalnych, natomiast kontynuacja może być prowadzona ambulatoryjnie.
Przy kwalifikacji pacjentów trzeba zawsze uwzględnić przeciwwskazania do rehabilitacji, a mianowicie: chorobę niedokrwienną serca, niewydolność krążenia, ostre serce płucne, znacznego stopnia zaburzenia funkcji wątroby, rak z przerzutami, udar mózgu, uzależnienie od narkotyków, ciężka choroba psychiczna.
Przed podjęciem właściwej rehabilitacji u już wstępnie zakwalifikowanych chorych, w celu określenia jej programu, trzeba wykonać dodatkowe badania. Przede wszystkim badania czynnościowe (spirometria spoczynkowa i po podaniu środka rozkurczowego), gazometrię spoczynkową, RTG klatki piersiowej, EKG i test wysiłkowy (ergometryczny na bieżni albo marszowy 6-12-minutowy). W razie potrzeby dodatkowo – morfologię, biochemię krwi.
Rzadko w razie konieczności wykonuje się badania czynnościowe po wysiłku fizycznym.
Podstawowymi elementami wszechstronnego programu rehabilitacji pneumologicznej są: ocena wydolności fizycznej, testy wysiłkowe i treningi. Korzyści wynikające z treningu wytrzymałościowego polegają na: zmniejszeniu duszności i poprawieniu sprawności czynnościowej, przywróceniu zdolności do wykonywania codziennych czynności i na ogólnej poprawie jakości życia. Ćwiczenia wysiłkowe zwiększają wytrzymałość, sprawność, zmniejszają ciśnienie krwi, przeciwdziałają depresji, pomagają w relaksacji – ułatwiają regulację glikemii, ułatwiają zasypianie.
Przeciwwskazania do testów wysiłkowych są bardziej restrykcyjne niż przeciwwskazania do rehabilitacji pneumologicznej, dlatego nie ma potrzeby ich omawiania w tym miejscu.
Próba wysiłkowa musi być dostosowana do stanu pacjenta, zadań programu, rodzaju ćwiczeń fizycznych, dostępnego sprzętu diagnostycznego i kosztów przeznaczonych na ten program. Na wyposażeniu pracowni niezbędny jest spirometr, aparat EKG, cykloergometr, ruchoma bieżnia, posiadanie zestawu pierwszej pomocy z defibrylatorem, pulsoksymetr, aparat do pomiaru ciśnienia, stetoskop, stoper, źródło tlenu, chodzik, wózek inwalidzki, zmierzony odcinek 30 metrów powierzchni i plan postępowania w stanach nagłych.
Najczęściej stosowanym testem w rehabilitacji pneumologicznej jest test marszowy – jako najprostszy i najtańszy w wykonaniu, a pod względem rezultatów jest porównywalny z innymi testami. Polega on na przejściu przez pacjenta pewnej odległości we właściwym dla niego tempie w czasie 6 lub 12 minut, ale częściej stosuje się marsz 6-minutowy.
Przed testem i po jego zakończeniu mierzy się tętno, ciśnienie krwi, saturację krwi O2, oblicza się prędkość marszu i wydatek energetyczny, ocenia się także nasilenie duszności oraz stopień zmęczenia wg 10-punktowej skali Borga.
Po zakończonym teście wykonuje się kontrolnie EKG, spirometrię oraz wysycenie tlenem krwi. U chorych z towarzyszącymi chorobami serca mogą się pojawić różnego rodzaju zmiany w zapisie EKG (obniżenie odcinka ST, zaburzenia rytmu itd.). U chorych z nadreaktywnością oskrzeli (astma, POCHP) mogą się nasilić objawy obturacji oskrzeli (powysiłkowy skurcz oskrzeli), dlatego wymagane jest wykonanie spirometrii.
Zdecydowanie można stwierdzić, że bez wykonania testów wysiłkowych przed i po programie rehabilitacyjnym, nie można byłoby obiektywnie ocenić skuteczności programu, opierając się tylko na subiektywnym odczuciu duszności i innych objawów klinicznych.
W wyniku choroby przewlekłej albo trwającej dość długo, ogólny stan pacjenta ulega pogorszeniu, a tolerancja wysiłkowa znacznemu zmniejszeniu.
W miarę nasilania się objawów chorobowych – częstych zaostrzeń – chory zaczyna prowadzić coraz to bardziej siedzący tryb życia, bo w taki sposób zapobiega przykremu nasileniu duszności. Niektórzy nazywają to „kołem” duszności albo „spiralą”: duszność powoduje zmniejszenie wydolności, czego przyczyną jest siedzący tryb życia, który z kolei ponownie nasila duszności, a te pogłębiają zaburzenia funkcji płuc, które wyrażają się w nasilonej i częstej duszności.
U chorych z nawet niezaawansowaną chorobą płuc w czasie prób wysiłkowych z maksymalnym obciążeniem występuje nasilona kwasica mleczanowa z towarzyszącą dodatkową reakcją wentylacyjną. Można oczekiwać, że wykonanie przez takiego chorego ćwiczeń z obciążeniem przekraczającym próg mleczanowy doprowadzi do fizjologicznych, korzystnych reakcji wytrenowania, czyli do zmniejszania się zapotrzebowania na wentylację na danym poziomie wysiłku i podwyższenia progu mleczanowego.
Ale mimo to, niezależnie od osiągnięcia lub nie progu beztlenowego w czasie próby wysiłkowej i ćwiczeń z narastającym obciążeniem, u chorych z przewlekłymi chorobami płuc, którzy biorą udział w programie rehabilitacji, obserwuje się zwiększenie wydolności wysiłkowej.
Dlatego jeśli nie ma przeciwwskazań, to u wszystkich chorych z przewlekłymi chorobami płuc wskazane są w ramach rehabilitacji pneumologicznej treningi i ćwiczenia fizyczne o różnej intensywności.
Program rehabilitacji musi być podzielony na kilka etapów: etap badań i określenia wydolności fizycznej, korekty farmakologicznej (który trwa od 2 do 5 dni), etap ćwiczeń fizycznych nadzorowanych w szpitalu rehabilitacyjnym, zakończony kontrolnym testem wysiłkowym. Ten etap trwa 3-4 tygodnie. Kolejny jest etap ambulatoryjny, kiedy pacjent w warunkach domowych wykonuje wyuczone ćwiczenia pod określoną kontrolą specjalisty. Ten etap trwa od 6 do 12 tygodni.
Jedna sesja ćwiczeniowa powinna zająć 30-45 min. W tym czasie mamy do wyboru następujące rodzaje ćwiczeń fizycznych: marsz na bieżni, jazdę na ergometrze rehabilitacyjnym (kończyny dolne), ćwiczenia dla kończyn górnych – unoszenie z obciążeniem lub bez, ćwiczenia na stopniach, wiosłowanie, aerobik w pozycji siedzącej (dla lepiej przygotowanych może być zmodyfikowany na stojąco).
Obowiązkowym warunkiem jest zażycie przepisanych leków przed rozpoczęciem ćwiczeń oraz obserwacja przez pacjenta reakcji swojego organizmu na intensywność ćwiczeń (przy pogorszeniu – natychmiast zaprzestać ćwiczeń). Rehabilitant prowadzący zajęcia ocenia stan pacjentów wg 10-punktowej skali Borga, która w postaci czytelnej tablicy musi znajdować się w polu widzenia ćwiczących. Ocena odczuwanych przez pacjentów dolegliwości wg tej skali pozwala w części przypadków przerwać ćwiczenia na wyznaczonym poziomie wysiłku, przy którym występują trudności w oddychaniu. A poziom ten zmienia się w zależności od przebiegu choroby odpowiedzialnej za wystąpienie duszności.
Na początku ćwiczeń ustala się mniej niż submaksymalny poziom intensywności ćwiczeń po to, aby przyzwyczaić chorego do wysiłku, a następnie, w miarę jak rośnie zaufanie chorego do programu ćwiczeń, zwiększa się w zakresie tolerowanym przez chorego czas trwania lub intensywność wysiłku.
W trakcie ćwiczeń kilkakrotnie kontroluje się nasycenie hemoglobiny tlenem (pulsoksymetrem, rzadziej poprzez określenie całkowitej gazometrii krwi), dlatego żeby określić zapotrzebowanie chorego na tlenoterapię. Zwykle zaleca się, żeby saturację Hb tlenem utrzymać powyżej 90 %.
Równolegle z treningiem wytrzymałościowym, opisanym powyżej, niezbędne jest prowadzenie treningu mięśni i treningu oddechowego. Ćwiczenia mięśni prowadzą do zwiększenia ich siły i wytrzymałości. Do treningu oddechowego należy zaliczyć: trening oddychania z oporem dla wydychanego powietrza (mniejsze otwory), z obciążeniem progowym dla wdechu oraz hiperwentylacją izokapniczną. Ćwiczenia z oporem muszą być wykonywane 4-5 dni w tygodniu z intensywnością 30-35% maksymalnego ćwiczenia wdechowego mierzonego w ustach.
Wyuczone w taki sposób ćwiczenia są przez pacjentów kontynuowane w domu, dzięki czemu utrzymują oni przez cały czas aktywność fizyczną poza formalnie nadzorowanym programem, realizowanym w Szpitalu Rehabilitacyjnym. Pacjent jest zobowiązany do prowadzenia w domu dzienniczka, gdzie zapisuje rodzaj ćwiczeń, ogólne samopoczucie, stan duszności (skala Borga), PEF (szczytowy przepływ wydechowy – mierzony pikflowetrem) oraz częstość zażywania środków farmakologicznych.
Zazwyczaj ćwiczenia zalecane do wykonywania w domu ocenia się pod kątem ich przydatności nie tylko w życiu codziennym, ale i w programie ćwiczeń podtrzymujących.
Korzyści płynące ze stałego stosowania ćwiczeń dla chorych z przewlekłymi schorzeniami układu oddechowego, to zwiększenie tolerancji duszności, poprawa apetytu, zwiększenie aktywności fizycznej oraz poprawa jakości życia.
Spis treści
Przede wszystkim należy ustalić priorytety i cele działania usprawniającego. Co chcemy osiągnąć w wyniku zastosowania rehabilitacji?
Najważniejszym celem jest ustabilizowanie już powstałych zaburzeń i w miarę możliwości ich odwrócenie, a jeżeli to nie jest możliwe, to przynajmniej zapobieganie gwałtownemu pogorszeniu stanu chorego i niedopuszczenie do powstania niewydolności oddechowej.
Do zasadniczych metod usprawniania w pneumologii należy zaliczyć:
gimnastykę ogólnousprawniającą z gimnastyką oddechową,
korygowanie nieprawidłowości postawy (przy zniekształceniach kręgosłupa i klatki piersiowej),
leczenie złożeniowe,
trening wytrzymałościowy,
stosowanie metod pomocniczych: masaż, elektroterapia, hydroterapia itd.
Gimnastyka ogólnousprawniająca polega na obustronnym równomiernym zaangażowaniu mięśni, co w sposób fizjologiczny przywraca pierwotną równowagę przy obciążeniu wysiłkiem.
Duże znaczenie w uzyskaniu pożądanego wyniku rehabilitacji ma odpowiedni sposób przeprowadzania ćwiczeń. Przed ich rozpoczęciem obowiązkowe jest rozluźnienie mięśni, co pozwala później skoncentrować uwagę pacjenta na zaangażowaniu odpowiedniej grupy mięśni i wyłączeniu tych, które przez swój skurcz uniemożliwiają przeprowadzenie w sposób prawidłowy ćwiczeń.
Rozluźnienie łatwiej uzyskuje się, gdy pacjent leży, dlatego ćwiczenia przyłóżkowe często rozpoczynają cały program rehabilitacji. Natężenie ćwiczeń też ma znaczenie – od początku ćwiczenia proste, mniej męczące stopniowo coraz bardziej wytężające, a przed końcem znów mniej męczące. Tempo ćwiczeń musi być dostosowane do indywidualnych możliwości pacjenta, określonych na podstawie testu wysiłkowego, ale pod warunkiem, że ćwiczenia wykonuje się przy miarowym i głębokim oddychaniu. Czas ćwiczeń 30-45 min jest rzadko wydłużany. Raczej wskazane są ćwiczenia wykonywane po południu, o mniejszej intensywności, trwające około 30 min.
Równolegle z ćwiczeniami ogólnousprawniającymi prowadzimy ćwiczenia oddechowe, wywołujące skurcze odpowiednich mięśni: przepony, mięśni międzyżebrowych zewnętrznych, mięśni brzucha – biorących bezpośredni udział w oddychaniu. W zależności od rodzaju ćwiczenia dzielą się na czynne (wykonywane samodzielnie), bierno-czynne (przy pomocy instruktora) i bierne (bez udziału pacjenta). Stosuje się także ćwiczenia z ruchem swobodnym – wolne albo oporowe – polegające na pokonywaniu przez grupę mięśni stawianego oporu.
Następnym właściwym elementem, stosowanym przy schorzeniach kręgosłupa, klatki piersiowej, po zabiegach torakochirurgicznych, są ćwiczenia korygujące nieprawidłowości postawy. Do tego rodzaju ćwiczeń należą ogólne ćwiczenia mięśni warunkujących prawidłową postawę; odpowiedniego ułożenia po zabiegu, ćwiczenia poprawiające ruchomość klatki piersiowej, zwiększające siłę mięśni klatki piersiowej i kręgosłupa.
Poprzez leczenie ułożeniowe rozumiemy odpowiednie ułożenie pacjenta (na boku z rotacją itd.), w wyniku czego możemy osiągnąć: prawidłowy odpływ wydzieliny z oskrzeli (drenaż), łatwiejsze rozprężenie płuca po zabiegu torakochirurgicznym oraz zapobieganie zniekształceniu kręgosłupa po zabiegu, niższe ustawienie przepony (wybiórczo), zwiększenie skurczu mięśni międzyżebrowych zewnętrznych, eliminację ruchów oddechowych danego odcinka klatki piersiowej (blokadami).
Duże znaczenie w usprawnianiu ruchowym pacjentów ze schorzeniami układu oddechowego odgrywają metody pomocnicze, takie jak masaż (klasyczny, rozluźniający i inny), elektroterapia: galwanizacja, ultradźwięki, magnetoterapia, laseroterapia itd., natomiast hydroterapia raczej w stopniu ograniczonym.
Rehabilitacja pneumologiczna przez długi czas skupiała się przeważnie na chorych z POCHP – najczęstszą postacią przewlekłych chorób płuc. Teraz sytuacja się zmienia, pojawia się coraz to więcej prac potwierdzających korzystny wpływ usprawniania ruchowego także u chorych z innymi schorzeniami płuc.
Ze względów praktycznych rehabilitację w chorobach płuc można podzielić na trzy grupy: w obturacyjnych chorobach płuc, w nieobturacyjnych chorobach i w innych.
Wśród obturacyjnych chorób płuc skupia się największa ich grupa: POCHP, astma oskrzelowa, niedobór p-antytrypsyny (rozedma), mukowiscydoza. Nieobturacyjne choroby to przede wszystkim schorzenia: śródmiąższowe choroby płuc, choroby opłucnej oraz przebiegające ze zmianami nerwowo-mięśniowymi i neurologicznymi z zajęciem mięśni oddechowych.
Do innych chorób płuc zaliczamy stany powstające po zabiegach torakochirurgicznych, po przeszczepie płuca, rak płuca, gruźlicę oraz choroby płuc występujące u dzieci.
Znajomość patofizjologii zaburzeń powstających przy CHOROBACH OBTURACYJNYCH (POCHP) jest nieodzowna do zrozumienia celowości ćwiczeń oddechowych, ich logicznego doboru i właściwego stosowania. Zaburzenia mechanizmu oddychania sprowadzają się do: ograniczenia ruchomości oddechowej klatki piersiowej, nieprawidłowego stosunku wdechu do wydechu, zmniejszenia ruchu oddechowego dolnożebrowego, nieprawidłowego uruchamiania górnych odcinków klatki piersiowej i ograniczenia oddechowej ruchomości przepony.
Tak jak już wspomniano – podstawowym elementem rehabilitacji jest wysiłek fizyczny, który nie tylko poprawia sprawność fizyczną chorego, ale i zmniejsza uczucie duszności, wpływa na samowystarczalność chorego, poprawia jego stan emocjonalny i jakość życia. Równolegle stosuje się gimnastykę oddechową i ćwiczenia ogólnousprawniające.
Najczęściej stosuje się 3-4-tygodniowy trening na ergometrze (bieżni mechanicznej), trwający 12-15 min, o intensywności powodującej przyspieszenie tętna do 115-120 uderzeń na minutę. Powoduje to w większości przypadków zmniejszenie wentylacji minutowej i zużycie tlenu przy takiej samej intensywności wysiłku.
Najprostszym sposobem sprawdzania skuteczności treningu fizycznego jest test 6-minutowego chodu, wykonany przed i po zakończeniu programu rehabilitacyjnego. W większości przypadków pokonana przez chorego odległość jest 10-15% większa niż przed programem.
Chorzy na POCHP często mają NADCIŚNIENIE PŁUCNE, które może znacznie wzrastać nawet przy niewielkim wysiłku fizycznym, natomiast systematyczny krótki wysiłek o średniej intensywności, jeśli w sposób znaczący nie poprawia hemodynamiki płucnej, to na pewno jej w sposób zasadniczy nie pogarsza.
Ćwiczenia mięśni oddechowych, szczególnie przepony, polegają na kontrolowanym oddychaniu z oporem równym co najmniej 30% maksymalnego ciśnienia wdechowego. Taki trening mięśni oddechowych zwiększa ich siłę i wytrzymałość.
Codzienny program ćwiczeń obejmuje:
ćwiczenia relaksacyjne (trening autogenny),
ćwiczenia rozluźniające i uruchamiające klatkę piersiową,
ćwiczenia oddechowe torem przeponowym,
ćwiczenia oporowego wydechu,
oklepywanie w pozycjach drenażowych i sprężynowanie klatki piersiowej,
ćwiczenia efektywnego kaszlu,
ćwiczenia oporowe kończyn górnych,
ćwiczenia ogólnousprawniające, trening na cykloergometrze z intensywnością wyliczoną podczas testu wysiłkowego,
zabiegi fizjoterapeutyczne (inhalacje, nebulizacje, naświetlania klatki piersiowej, elektroprocedury, masaż klasyczny).
Program tworzy się indywidualnie, w stosunku do konkretnego pacjenta, uwzględniając ww. propozycje testów i ćwiczeń.
Omawiany program jest modyfikowany i uzupełniany w zależności od jednostki chorobowej.
W ASTMIE OSKRZELOWEJ należy uwzględnić, iż przed planowanym wysiłkiem obowiązkowo trzeba zażyć leki zapobiegające powysiłkowemu skurczowi oskrzeli oraz przeprowadzić kontrolny pomiar szczytowego przepływu wydechowego (PEF). W trakcie rehabilitacji natomiast – przeanalizować i w miarę możliwości wykluczyć czynniki wyzwalające napad duszności, jak i ustosunkować się do diety dla chorych leczonych przewlekle kortykosteroidami.
Ważny i zasługujący na podkreślenie jest fakt, iż spokojny głęboki oddech ma działanie bronchodilatacyjne (rozszerzające oskrzela), w przeciwieństwie do hiperwentylacji, która ma działanie bronchokonstrukcyjne (zwężające oskrzela), wyzwalające napad duszności.
Niezbędna jest edukacja i szkolenie chorego dostosowane do jego wieku oraz stworzony plan samodzielnego leczenia pacjenta w warunkach domowych.
Powikłania oddechowe spowodowane zaleganiem śluzu i nawracającymi zakażeniami dróg oddechowych są główną przyczyną pogarszania się czynności płuc u chorych na genetycznie uwarunkowaną chorobę, jaką jest MUKOWISCYDOZA.
Zasadniczym leczeniem w mukowiscydozie jest terapia genetyczna (w przyszłości) albo przeszczep. W programie usprawniania ruchowego należy uwzględnić: drenaż ułożeniowy, ćwiczenia kaszlu kontrolowanego, ćwiczenia siłowe i zwiększające wytrzymałość, dietę i stan żywienia. Podczas występowania wysokich temperatur otoczenia trzeba uzupełniać sód i chlorki. Ważne jest także to, żeby pacjent rozumiał sens i konieczność programu, a rodzina, po przeszkoleniu, stanowiła grupę wsparcia dla niego.
W śródmiąższowych chorobach płuc o różnej etiologii (SARKOIDOZA, idiopatyczne zwłóknienie płuc, pylica) podstawowym objawem jest duszność, która w miarę szybko z wysiłkowej przekształca się w spoczynkową. W związku z tym program usprawniania musi opierać się na ocenie zapotrzebowania na tlenoterapię, tlenoterapii właściwej, oraz na wysiłku fizycznym uzależnionym od zdolności do zachowania odpowiedniego utlenowania krwi.
Należy podkreślić, iż w śródmiąższowych chorobach płuc mechanika oddychania jest skuteczna przy mniejszych objętościach oddechowych i częstych oddechach. Nauka głębokiego oddychania jest w tych przypadkach błędem. Szczególnie ważny dla pacjentów ze śródmiąższowymi chorobami płuc jest kontakt z psychologiem klinicznym, ze względu na krótki okres przebiegu choroby, prowadzącej do niepełnosprawności.
Postępowanie rehabilitacyjne zaczyna się już w szpitalu, a następnie kontynuuje się je ambulatoryjnie. W WYSIĘKOWYM ZAPALENIU OPŁUCNEJ i w zapaleniu płuca z odczynem opłucnowym postępowanie to sprowadza się do 2 zasadniczych metod: leczenia ułożeniowego oraz gimnastyki oddechowej.
W pierwszym okresie, gdy chory gorączkuje i stwierdza się obecność płynu w opłucnej, układa się pacjenta na zdrowym boku, mimo odczuwania przez niego bólu w klatce piersiowej po stronie chorej, którą oszczędza on podczas oddychania i wykonywania ruchów. Takie ułożenie powoduje przyspieszenie wchłaniania płynu z opłucnej i zapobiega wytrącaniu się złogów włóknika na opłucnej, a tym samym wytwarzaniu się zrostów przeponowo-opłucnowych.
Po ustąpieniu ostrego okresu choroby i leczeniu ułożeniowym, przystępuje się do ćwiczeń mięśni oddechowych, zwłaszcza przepony. Na brzuchu układa się woreczek z piaskiem 1,5-5 kg. Ćwiczenia przepony w postaci wdechu i wydechu pacjent wykonuje kilka razy w ciągu dnia.
Następnym etapem jest wykonywanie ćwiczeń na sali gimnastycznej, kontynuujące ćwiczenia mięśni brzucha, oddychania dolnożebrowego, ćwiczenia mięśni obręczy barkowej i ogólnousprawniających.
Po rozpoczęciu ćwiczeń na sali pacjent przystępuje do treningu fizycznego o intensywności określonej przez test marszowy. Wyniki ocenia się na podstawie powrotu parametrów spirometrycznych do normy (VC, FEV1) oraz prawidłowej ruchomości przepony.
Usprawnianie ruchowew TORAKOCHIRURGII dzieli się na postępowanieprzed- i pooperacyjne. Ćwiczenia stosowane przed zabiegiem chirurgicznym, poza korzyściami fizjologicznymi, przywracają znaczną korzyść psychologiczną – pacjent nabiera wiary w pomyślny przebieg zabiegu i w to, że zabieg nie wpłynie na jego wygląd, zniekształcając mu w sposób znaczący kształt klatki piersiowej, jak i w to, że nie rozwinie się po zabiegu niewydolność oddechowa (zwłaszcza po rozległych operacjach).
Cele, które muszą być osiągnięte po zastosowaniu rehabilitacji, są następujące: korekta istniejących przed zabiegiem zaburzeń mechanizmu oddychania, zapobieganie następstwom samego zabiegu chirurgicznego, leczenie powstałych po zabiegu nieprawidłowości, jak np. w zakresie układu kostnego, mięśni oraz mechanizmu oddychania.
Przed zabiegiem pacjent wykonuje ćwiczenia oddychania przeponowego oraz oddychania dolnożebrowego, ćwiczenia mięśni obręczy barkowej oraz ćwiczenia ogólnousprawniające. Bezpośrednio przed zabiegiem zasadnicze znaczenie ma nauka efektywnego kaszlu. Pacjent jeszcze przed zabiegiem musi nauczyć się radzić sobie z wykrztuszaniem, gdyż po zabiegu – ze względu na bóle – nie będzie mógł nauczyć się prawidłowego wykonywania nowych dla niego ćwiczeń.
Rehabilitacja w okresie pooperacyjnym dzieli się na: wczesną – już w pierwszym dniu po zabiegu i właściwą – 10-12 dni po zabiegu. Wczesną prowadzi się na oddziale torakochirurgicznym, a właściwą w Specjalistycznym Ośrodku – wyposażonym w odpowiedni sprzęt i zatrudniającym wielospecjalistyczny zespół przygotowany na wszechstronne rozwiązywanie problemów, które powstają po mniej lub bardziej traumatycznym zabiegu u danego pacjenta – współpracującym z oddziałem chirurgicznym.
Podobnie jest zorganizowany przebieg rehabilitacji w Wielkopolsce. Pacjent zostaje zoperowany przez zespół chirurgów pracujących w Wielkopolskim Centrum Chorób Płuc w Poznaniu, gdzie rozpoczyna się rehabilitacja pooperacyjna. Natomiast drugi jej etap odbywa się w Wojewódzkim Specjalistycznym Szpitalu Gruźlicy i Chorób Płuc w Ludwikowie na oddziale rehabilitacyjno-pulmonologicznym dla dorosłych.
Zabieg operacyjny działa stresogennie nie tylko pod względem somatycznym, ale i psychicznym. Występują bóle w okolicy rany, osłabienie, duszność, która w pewnym stopniu izoluje pacjenta od otoczenia.
Niewątpliwie bardzo ważnym zadaniem jest właściwe postępowanie podczas kaszlu u pacjenta będącego po zabiegu. Zalegająca wydzielina, zmieszana z krwią, może stać się powodem niebezpiecznych powikłań. Dobre wyniki uzyskuje się przy starannym ułożeniu pacjenta, w celu uzyskania lepszego oczyszczania oskrzeli podczas kaszlu.
Prawidłowe ułożenie chorego w łóżku zapobiega też pewnego rodzaju nawykom powodującym wtórne zniekształcenie klatki piersiowej i kręgosłupa w późniejszym okresie.
Ważne jest wznowienie ćwiczeń oddychania przeponowego z oporem stawianym ręką instruktora przy wdechu oraz ćwiczeń ogólnych z ruchami w drobnych stawach. Pokonanie progów bólowych pozwala na wcześniejsze uruchomienie barków.
Następnym ważnym elementem rehabilitacji pooperacyjnej jest zapobieganie zaburzeniom statycznym kręgosłupa oraz zniekształceniom klatki piersiowej i ich korekta (ograniczenie ruchomości barku z mobilizacją łopatki, leczenie zaników mięśni szyi itd.).
Rehabilitacja pneumologiczna po operacyjnym leczeniu schorzeń płuc musi być prowadzona nie tylko według zasad kinezyterapii, ale także wg ogólnych zasad rehabilitacji, w myśl których badanie tolerancji wydolności fizycznej poprzedza program rehabilitacyjny i kończy okres stacjonarnej rehabilitacji, mając na celu określenie zmian w zakresie skuteczności leczenia farmakologicznego i zapotrzebowania na tlenoterapię. W późniejszym terminie stosowany jest trening fizyczny na ergometrze rowerowym albo bieżni ruchowej.
Zupełnie inaczej przedstawia się program rehabilitacji w RAKU PŁUCA.Samo rozpoznanie i leczenie zasadnicze wywołuje wiele fizycznych i psychologicznych problemów,m.in. ograniczenie wydolności fizycznej aż do niemożliwości wykonywania codziennych czynności, depresji, duszności, lęku.
Zaburzenia oddechowe w postaci kaszlu, duszności mogą występować przy zwężeniu tchawicy, oskrzeli z powodu obecności guza, uszkodzenia tkanki płucnej w wyniku radio- albo chemioterapii. Celem takiego programu jest przede wszystkim poprawa sprawności i jakości życia tych pacjentów.
W programie rehabilitacyjnym pacjentów z rakiem płuca uwzględnia się przede wszystkim optymalne leczenie farmakologiczne oraz przerwanie programu w razie pojawienia się dodatkowych możliwości leczenia podstawowego.
Następnym elementem programu jest wysiłek fizyczny o małej intensywności, ale systematyczny i bezpieczny dla chorego.
Program nie będzie pełny bez uczestnictwa w nim psychologa klinicznego. Pacjent boryka się z ciągłym poczuciem niepewności dnia jutrzejszego, prześladują go lęki i obawy o los bliskich, co może doprowadzić do ciężkiej depresji, a w takim momencie większość pacjentów z ra-kiem płuca rezygnuje z leczenia.
Pacjenta trzeba stale przekonywać do ćwiczeń fizycznych, tłumacząc wynikające z nich korzyści oraz z perspektywy lepszego samopoczucia, jak i z lepszej jakości życia. Dobrze, kiedy program jest prowadzony we współpracy z rodziną chorego, która włącza się w ćwiczenia i wspiera chorego w jego dążeniu do zdrowia.
Czasami zdarza się, że pacjent w trakcie chemioterapii albo radioterapii nie jest w stanie z powodu ubocznych działań tych zabiegów uczestniczyć w programie w pełni. Instruktor stosuje wtedy zmodyfikowany program: ćwiczenia relaksacyjne, oddechowe, metody oszczędzania energii. Ustala indywidualne tempo podejmowania aktywności przez chorego.
Nie wyklucza się udziału pacjenta z rakiem płuca w pełnym programie rehabilitacji pneumologicznej po ustąpieniu dolegliwości i określeniu jego wydolności fizycznej oraz stopnia duszności (wg skali Borga). Ten program jest porównywalny z programem po zabiegach torakochirurgicznych i skierowany jest na zwiększenie siły mięśniowej oraz wytrzymałości.
Po zakończonej radioterapii w płucach powstają zmiany włókniste, jak w chorobach śródmiąższowych płuc, co wymaga wprowadzenia dodatkowego leczenia i innego aspektu rehabilitacji tych chorych. Może również zdarzyć się sytuacja, że po kilku latach leczenie sprowadza się nie do walki z chorobą nowotworową, a z postępującymi zmianami śródmiąższowymi.
W rezultacie przeprowadzonych badań, leczenia i rehabilitacji pacjent z rakiem płuca ma być przeszkolony i wyedukowany przez wielospecjalistyczny zespół do samodzielnego radzenia sobie z dolegliwościami fizycznymi i psychologicznymi, powstającymi w przebiegu schorzenia.
Wojewódzki Specjalistyczny Szpital Gruźlicy i Chorób Płuc znajduje się na terenie Wielkopolskiego Parku Narodowego i zajmuje powierzchnię 50 hektarów lasu mieszanego, przeznaczoną na działalność leczniczo-rehabilitacyjną. Właścicielem terenu jak i budynków jest Samorząd Województwa, a właściwie Marszałek Województwa Wielkopolskiego. Organem założycielskim Szpitala jest Sejmik, który nadzoruje Szpital poprzez wyznaczoną czteroosobową Radę Społeczną.
Szpital jest zarejestrowany w Sądzie Rejonowym i w Rejestrze Wojewody Wielkopolskiego jako Samodzielny Publiczny Zakład Opieki Zdrowotnej od 1996 r.
W skład Szpitala wchodzą: 2 pawilony lecznicze, 1 administracyjny, 4 mieszkalne, portiernia, kaplica, stacja pomp przy studniach, oczyszczalnia ścieków, zespół szklarni, strzelnica myśliwska.
W Pawilonie leczniczym nr I, u zbiegu ulic Lipowej i Leśnej – znajduje się na parterze dział diagnostyczny: laboratorium analityczne, bakteriologiczne, pracownia RTG, sala bronchoskopowa, a poza tym sala komputerowa, pomieszczenie szkoły (dla leczących się dzieci), sala konferencyjna, sala obrad. Na I piętrze znajduje się oddział leczenia gruźlicy z pododdziałem leczenia gruźlicy wielolekoopornej – łącznie 50 łóżek. Oddział posiada własne inhalatorium i pracownię czynnościową z gabinetem EKG oraz salę gimnastyczną wyposażoną w różnorodny sprzęt rehabilitacyjny. Na II piętrze znajduje się oddział rehabilitacyjno-pul-monologiczny dla dzieci i młodzieży na 20 łóżek, gdzie oprócz pokoi tematycznie opracowanych przez plastyka („świat podwodny”, „ogród bajkowy”, „sala egipska” i inne) znajduje się własne zaplecze fizjoterapeutyczne i gabinet zabiegowy, a także świetlica.
W Pawilonie leczniczym nr II przy ul. Parkowej znajduje się w piwnicy: punkt przyjęć, punkt konsultacyjny, pracownia USG, inhalatornia, sala rehabilitacyjna nr 1 do ćwiczeń w odciążeniu, sala nr 2 wyposażona w 7 stołów do masażu różnych części ciała z napędem elektrycznym i apteka szpitalna. Na parterze znajduje się oddział pulmonologiczny na 30 łóżek z gabinetem zabiegowym, sala intensywnego nadzoru, sala gimnastyczna nr 3 dla ćwiczeń grupowych, gabinet fizjoterapii wyposażony m.in. w aparaty do magnetoterapii, laseroterapii, ultradźwięki. Na I piętrze umiejscowiony został oddział rehabilitacyjno-pulmono-logiczny dla dorosłych na 30 łóżek, gdzie oprócz gabinetu zabiegowego, świetlicy do grupowej psychoterapii znajduje się pracownia testów wysiłkowych i badań czynnościowych Akademii Wychowania Fizycznego im. E. Piaseckiego w Poznaniu, wyposażona w kompletny skomputeryzowany sprzęt do przeprowadzania testów wysiłkowych na ergometrze rowerowym z jednoczesnym wykonaniem EKG i badaniem parametrów spirometrycznych. Na II piętrze znajduje się oddział długoterminowej opieki onkologicznej z pododdziałem laryngologicznym, gdzie są leczeni pacjenci z rakiem płuca, rakiem krtani i jamy ustnej, którzy są dowożeni karetkami do Wielkopolskiego Centrum Onkologii na radioterapię. Pacjentami oddziału, oprócz lekarzy – pneumologów, opiekuje się konsultant-laryngolog oraz szpitalny psycholog kliniczny.
Na każdym z oddziałów znajduje się biblioteka dla pacjentów, a w świetlicach są telewizory. Jest także możliwość wypożyczenia gier planszowych.
Na terenie szpitalnego parku, w cienistym zakątku przy ul. Leśnej, znajduje się kaplica szpitalna, zmodernizowana w 2002 r., z własną dzwonnicą.
Niedaleko Pawilonu leczniczego nr I, pośrodku ścieżek spacerowych, przy zabytkowych leżakowniach, znajduje się figura Matki Bożej, a obok tegoż Pawilonu przy ul. Parkowej – figura Pana Jezusa, postawiona przy udziale parafii mosińskiej w roku 75 rocznicy założenia Szpitala.
W środku parku wybudowana została altana z pijalnią wody źródlanej mineralnej, o wybitnych walorach smakowych, z niską zawartością sodu, pod nazwą „Ludwiczanka”.
Park przecinają wyłożone płytką chodnikową drogi spacerowe, zaopatrzone w drogowskazy pozwalające bez przeszkód trafić do każdego z wyznaczonych na mapie punktów. Plan Ludwikowa znajduje się przy wjeździe na teren Szpitala, obok pamiątkowego głazu z tablicą okolicznościową wmurowaną z okazji 75-lecia powstania Szpitala.
Do Wojewódzkiego Specjalistycznego Szpitala Gruźlicy i Chorób Płuc w Ludwikowie trafiają pacjenci z całej Wielkopolski, ale przeważnie z dużych poznańskich szpitali, takich jak Wielkopolskie Centrum Chorób Płuc, Wojewódzki Szpital Zespolony przy ul. Lutyckiej, Szpital MSW, Wielkopolskie Centrum Onkologii, ze Szpitali Klinicznych nr 1, 2, Szpitala im. F. Raszei i Szpitala HCP.
W Szpitalu są leczeni pacjenci z całą gamą schorzeń układu oddechowego, czemu służą nie tylko panujące tam wspaniałe warunki klimatyczne, ale i doskonale przygotowany wykwalifikowany personel wielo-specjalistycznego zespołu pracowników oraz specjalnie dobrany dla tej grupy pacjentów sprzęt leczniczo-rehabilitacyjny.
Pacjenci są przywożeni do Szpitala karetkami sanitarnymi, a rodziny odwiedzające chorych mogą dojechać tutaj albo autobusami PKS z Poznania przez Luboń, Puszczykowo i Mosinę (rano i w południe), jak i środkami PKP do Mosiny.
W roku 2002 Szpital w Ludwikowie został odznaczony Odznaką Honorową Marszałka Województwa „Zasłużony dla Województwa Wielkopolskiego” za osiągnięcie wysokich rezultatów w świadczeniu usług medycznych dla mieszkańców województwa wielkopolskiego.
W roku 2003 ludwikowskiej Lecznicy został przyznany certyfikat Jakości ISO 9001:2001 w dziedzinie diagnostyki, leczenia, rehabilitacji i pielęgnacji nieswoistych chorób układu oddechowego, co w sposób zdecydowany podkreśliło znaczenie i poziom usług świadczonych w Wojewódzkim Specjalistycznym Szpitalu Gruźlicy i Chorób Płuc w Ludwikowie na rzecz mieszkańców Wielkopolski i jej stolicy Poznania.
American Thoracic Society Standards for the diagnosis and care of patients with chronic obstructive pulmonary disease (COPD). Am J Respir Crit Care Med 1995, 152 (Suppl.5), 77-120.
Barinow-Wojewódzki A., Specjalistyczny Szpital Chorób Płuc i Gruźlicy w Ludwikowie. Print. Ludwikowo 1999.
Barinow-Wojewódzki A., Prezentacja walorów powietrza atmosferycznego terenów Szpitala Chorób Płuc w Ludwikowie na tle miasta Poznania. I Konferencja Naukowa w Ludwikowie: „Standardy postępowania w leczeniu, rehabilitacji i pielęgnacji pacjentów z chorobami układu oddechowego”. AWF, Poznań 2003, 8-14.
Barlet Jon G., Leczenie zakażeń układu oddechowego. Kraków 1999.
Chórek-Borowska S. (red.), Farmakoterapia chorób alergicznych. PZWL, Warszawa 1993, 132-153.
Droszcz W., Astma. Zarys patofizjologii, zasady diagnostyki i leczenia. PZWL, Warszawa 2002.
Dudiey D/L, Wermuth C., Hague W., Psychosocial aspects of care in the chronic obstructive pulmonary disease patient. Heart Lung, 1973, 2, 289.
Hodgkin J.E., Benefits of pulmonary rehabilitation. [W:] Pulmonary rehabilitation. Edited by A.P. Fishman, 1996, 33-53, New York: Marcel Dekker.
Kochanowicz I., Lecznicza rehabilitacja oddechowa w chorobach płuc. PZWL, Warszawa 1972.
Limanowski A. (red.), Choroby układu oddechowego. PZWL, Warszawa 2000.
Mal H., Chirurgia zmniejszająca objętość płuc. American Thoracic Society. San Francisco, USA, 18-23 maj 2001.
Mal H., Zapalenie dróg oddechowych przebiegu POCHP. American Thoracic Society. San Francisco, USA, 18-23 maj 2001.
Novitch R.S., Thomas H.M., Pulmonary rehabilitation in patients with interstitial lung disease. Am Rev Respir Dis, 1995, III. A684.
Novitch R.S., Thomas H.M., Pulmonary rehabilitation in chronic pulmonary interstitial disease. [W:] Pulmonary rehabilitation, Lung biology in health and disease. Edited by A.P. Fishman, 1996, Vol. 91, 683-700, New York: Marcel Dekker Inc.
Prefant C., Osłabienie tolerancji wysiłku fizycznego jako skutek zaburzeń czynności mięśni obwodowych. American Thoracic Society. San Francisco, USA, 18-23 maj 2001.
Punzal P.A. et al., Maximum intensity exercise training in patients with COPD. Chest 1991, 100, 618-623.
Ries A.L., Effects of pulmonary rehabilitation on physiologic and psychosocial outcomes in patients with chronic obstructive pulmonary disease. Ann Inter Med 1995, 122, 823-832.
Ries A.L., The importance of exercise in pulmonary rehabilitation. Clin Chest Med, 1994,15 (2), 327-337.
Roszkowski K., Drobnokomórkowy rak płuca. Instytut Gruźlicy i Chorób Płuc, Warszawa 1993.
Rowińska-Zakrzewska E. i wsp., Choroby śródmiąższowe płuceeee- media press, Bielsko-Biała 2001.
Rowińska-Zakrzewska E., Kuś I. (red.), Choroby układu oddechowego. PZWL, Warszawa 1997.
Rowińska-Zakrzewska E. (red.), Gruźlica w praktyce lekarskiej. PZWL, Warszawa 2000.
Sładek K., Alergia dolnych dróg oddechowych. [W:] Alergia praktyczna, red. K. Obtułowicz. PZWL, Warszawa 2001.
Smith K. et al., Respiratory muscle training. Thorax 48, 1025-1033.
Straburzyński G., Leczenie uzdrowiskowe w fizjoterapii. PWN, Warszawa 1988, 328-343, 347, 445-449.
Steele B., Time walking tests of exercise capacity in chronic cardiopulmonary illness. L Cardiopulm Rehabil, 1995, 16, 25.
Sutton F.D., The propriety of pulmonary rehabilitation program. [W:] Principles and practice of pulmonary rehabilitation. Edited by R. Casaburi and T.L. Petty, 1993, Philadelphia: W.B. Saunders.
Weaver T., Narsavage G., Physiological and psychological variables related to functional status in chronic obstructive pulmonary disease. Nurs Res 1992, 41, 286-291.
Wojciechowicz H., Usprawnienie chorych ze schorzeniami układu oddechowego. Rehabilitacja medyczna pod red. K. Limanowskiej. PZWL, Warszawa 2001, 512-520.
Zieliński J. i wsp., Przewlekła obturacyjna choroba płuc. PZWL, Warszawa 1999.